| Tabela 2 - Índice histológico de atividade da doença |
 |
ARTIGOS ORIGINAIS
ROBERTO AMARAL - TSBCP
ANTÔNIO DAL PIZZOL JR.
CIRO PAZ PORTINHO
PAULO BRAGA
LUIS FERNANDO MOREIRA
PEDRO GUS TSBCP
resumo: A procura de alternativas no tratamento da colite ulcerativa tem sido estimulada em função das falhas das terapias convencionais e dos avanços no entendimento dos múltiplos mecanismos que envolvem a sua etiopatogenia .
Objetivo: verificar a eficácia de enemas de ciclosporina (CyA) no tratamento da colite ulcerativa induzida experimentalmente por ácido acético em ratos e, secundariamente, desenvolver um modelo experimental de colite induzida em nossa Instituição.
Material e métodos: realizou-se um ensaio clínico, randomizado, unicego, controlado por placebo utilizando-se 55 ratos (Wistar)
divididos em 4 grupos: A (n=15, indução com ácido acético 7%), B (n=16), indução com ácido acético + enemas de CyA/2,0 mg/kg/6 dias),
C (n=9, indução com solução fisiológica + enemas de CyA/0,5 mg/6 dias) e D (n=15, indução com solução fisiológica).
Variáveis de interesse: alterações macro e microscópicas da mucosa colônica e modificações diárias no peso, ingesta alimentar
e características das fezes dos animais.
Resultados: durante o estudo (14 dias), sacrificaram-se exemplares de cada grupo nos dias 2, 3, 5, 7 e 14 para avaliações macro e microscópicas. Não foram observadas alterações estatiscamente significativas das variáveis peso, ingesta alimentar e características das fezes quando se compararam os grupos A e B. A avaliação macroscópica foi significativa na comparação dos grupos A e B tanto no período acumulado do 2º ao 14º dia (p=0,037) como do 3º ao 14º dia (p=0,009). O Índice histológico da atividade da doença (IHAD) não mostrou diferença estatisticamente significativa quando da comparação dos grupos A e B (média=1,27 vs 1,75).
Conclusão: o modelo de indução experimental da colite por ácido acético a 7% é eficaz e reprodutível; a via de administração foi segura quando consideradas a ausência de alterações no peso, ingesta e características das fezes; a dose de 2,0 mg/kg/dia mostrou eficácia ao modificar positivamente as alterações macroscópicas da mucosa colônica não sendo capaz de apresentar os mesmos resultados quando avaliados histologicamente.
UNITERMOS: colite ulcerativa, colite induzida quimicamente, terapia, imunossupressão, ciclosporina
Nos últimos anos, uma das doenças mais estudadas
tem sido a colite ulcerativa. Tal interesse deriva de suas
variadas formas de apresentação, do crescente número de
diagnósticos nos últimos anos, da importante
morbimortalidade e de seu elevado custo
social1-4.
O marcado aumento no risco de câncer colorretal,
chegando em alguns estudos a uma incidência cumulativa
em 35 anos de até 25 % em pacientes com
pancolite5-8 e o grau de incapacidade que a doença pode
trazer9 reforçam a relevância do assunto e a necessidade crescente da
investigação nesta área.
O tratamento da colite ulcerativa encontra-se
restrito pela sua patogênese obscura e pelo limitado
entendimento dos eventos imunoinflamatórios que a desencadeiam.
Até o momento, a intervenção terapêutica concentra-se,
principalmente, no combate às conseqüências da
amplificação das cascatas imunológicas e inflamatórias e às
repercussões sistêmicas destas. O entendimento, ainda que
incompleto, destes mecanismos tem proporcionado o
desenvolvimento de linhas de pesquisa. Desta maneira, além
dos tratamentos já consagrados (aminossalicilatos e
glicocor-ticóides) avalia-se a utilização de imunomoduladores,
ina-tivadores de radicais livres, inibidores da síntese de
leuco-trienos e de inibidores do recrutamento de neutrófilos
entre outros10,11,12.
Modelos mais elaborados de pesquisa apresentam
inúmeras dificuldades seja na operacionalização,
possibilidade de vieses, dificuldade de extensão de suas
conclusões ou pelo custo e tempo de realização. Neste contexto,
os modelos experimentais de indução de colite, guardadas
as suas limitações, podem servir como alternativas viáveis
para estudar sua etiopatogenia ou mesmo seu manejo
tera-pêutico13. Existem vários modelos de indução da colite
(ácido acético, ácido trinitrobenzenosulfônico,
carragenam/sulfato dextram, imunocomplexos, indometacina,
tamarin, HLA-B27)14-22. Dentre estes, o de indução tóxica pelo
ácido acético, inicialmente proposto por MacPherson e
cols14, tem sido muito utilizado pela praticidade e
apresentação aguda da doença. Existem vários métodos de
administração do ácido acético: (1) aplicação tópica na
serosa14; (2) injeção intraluminal através de ceco
previamente isolado e lavado com uma solução
tamponada15 (3) instilação
em um segmento colônico exteriorizado por duas
colostomias18 ou (4) através de enemas por cateter introduzido de 3,0
a 8,0 cm da borda anal14,16,17,19. As concentrações e os
volumes de ácido acético variam de 4 a 50% e de 1,0 a 2,0
mL respectivamente enquanto os tempos de permanência
do ácido também variam de segundos até
horas14-19. A concentração utilizada determina a intensidade das lesões
observadas. As lesões apresentam-se mais intensas,
tanto macro como microscopicamente, na primeira semana
apresentando recuperação praticamente completa ao final
da segunda semana15-19.
Embora seja um modelo claramente tóxico, é
provável que a resposta inflamatória resultante seja devida ao
produto do influxo de conteúdo luminal para a lâmina
própria decorrente da destruição das células epiteliais com
perda da barreira epitelial entre as células imunológicas da
lâmina própria e os antígenos do lúmen. E, apesar de
diverso daquele que se encontra na colite ulcerativa, onde o
evento iniciador é uma ativação das células imunológicas da
lâmina própria que levam a um dano das células epiteliais,
ambas as situações mostram uma surpreendente semelhança
quando se examina o padrão do metabolismo do
ácido aracdônico. Na duas situações tanto os produtos
da lipoxigenase como da cicloxigenase são igualmente
dependentes da infiltração dos neutrófilos, seja na colite
ulcerativa ou na mediada pôr ácido
acético16,18,23. Como a colite induzida é precoce e aguda é possível sua utilização
no estudo desta fase da doença a fim de investigar qual
ou quais componentes da doença inflamatória intestinal
são produtos de um componente inflamatório agudo bem
como avaliar a eficácia farmacológica de novas drogas nesta
fase da doença.
As propriedades imunossupressivas da
ciclosporina (CyA), descritas inicialmente por Borel e
cols24 em 1976, e conhecimento de que as doenças inflamatórias
intestinais sejam etiologicamente imunomediadas fez crescer o
interesse por seu uso nesta área desde
198410,11. Ela difere dos imunossupressores convencionais pelo fato de não
apresentar influência significativa sobre as funções
hema-topoiética, fagocítica e neoplástica. A CyA possui um
efeito seletivo, reversível e desconhecido principalmente
na indução dos linfócitos T-auxiliares
(helper) que comandam a resposta imune antígeno dependente. Sua ação
se dá na interferência da proliferação e da função
linfocítica, principalmente, através da inibição da transcrição
da Interleucina-2 (IL-2)10,12,25 bloqueando a liberação desta
e de outras linfocinas ao mesmo tempo que deixa intacta
a expressão dos receptores para IL-2 e a responsividade
das células T ativadas às linfocinas circulantes. Ela pode
ainda afetar outras células da lâmina própria e da circulação
periférica através do efeito da droga sobre as células T e
as citocinas além de também inibir a ativação de mastócitos
e a degranulação de basófilos. Não se evidencia nenhum
efeito da droga sobre as células B ou os macrófagos. A
resposta supressora máxima da proliferação linfocítica se
dá quando a droga é dada nas primeiras 24 h de exposição
ao estímulo. A medida que o tempo entre a exposição e
a administração aumentam, a proliferação
diminui marcadamente10. Quanto aos efeitos adversos, a CyA é
uma droga potencialmente tóxica salientando-se
nefro-toxicidade, hipertensão, hipertricose, parestesias/tremores,
hepa-totoxicidade, hiperplasia gengival e
náuseas12. Dentre estes, a nefrotoxicidade é o mais importante ocorrendo com
maior freqüência se houver a concomitância com outras
drogas nefrotóxicas. Há reversão, em aproximadamente 90%
dos casos, após a suspensão da
droga10. Alterações
linfopro-liferativas são menos freqüentes do que as observadas
com os imunossupressores
convencionais10,12,25. Infecções
opor-tunísticas podem ocorrer quando se usam doses altas
da droga (> 5,0 mg/kg/dia/VO ou 4,0
mg/dia/IV)26.
Se o início precoce dos efeitos positivos é uma
vantagem, os efeitos adversos e as falhas na manutenção
da remissão pós tratamento são óbices para seu
uso11,27. Vários estudos não-controlados mostraram a eficácia da
droga, no tratamento de casos graves de colite ulcerativa,
quando administrados pelas vias oral e
intravenosa27. Nos casos
refratários de colite esquerda e distal a administração
de CyA pela via retal tem sido testada na tentativa de
se minimizar seus efeitos adversos. Pontos a favor da
administração de enemas em solução aquosa vêm da sua
eficácia local, de níveis teciduais colônicos até 10 vezes
maiores do que os obtidos com a via oral, semelhantes
àqueles pós administração IV, além da vantagem da
concentração plasmática
baixa10,12. Isto ocorre porque a forma
aquosa diminui a absorção da CyA evitando-se os efeitos
adversos de concentrações séricas
elevadas28. Estudos
experimentais29, utilizando doses de 2,5 a 10,0 mg/kg e estudos
abertos30,31, com doses variando de 250,0 a 350,0 mg/dia,
testaram esta hipótese encontrando resultados positivos
em mais de 50% dos casos. Existem relatos de que
existiria ainda uma correlação positiva entre a resposta e o
tempo de retenção do
enema11.
O objetivo principal deste estudo foi verificar a
eficácia de enemas de ciclosporina (CyA) no tratamento de
colite ulcerativa induzida por ácido acético tendo-se
como parâmetros de avaliação as alterações macro e
microscópicas da mucosa colônica bem como as modificações
no peso, ingesta alimentar e características das fezes.
Secundariamente, objetivou-se desenvolver em
nossa Instituição um modelo de indução experimental de colite,
a partir da utilização de enemas de ácido acético, de
baixo custo e fácil realização.
MATERIAL E MÉTODOS
O estudo foi conduzido em consonância com os
princípios estabelecidos pelo "Guide for care and use of
laboratory animals" (Institute of Laboratory Animal
Resources, National Research Council, Washington DC, 1996).
Realizou-se um ensaio clínico, randomizado,
unicego, com controle interno, onde os controles recebiam ou
enema de solução fisiológica, no mesmo volume usado para
a indução, ou enemas diários de ciclosporina, na mesma
dose e mesmo período usados no grupo intervenção.
A técnica escolhida para a indução da colite foi
uma adaptação daquelas descritas por Yamada e
cols16 e Tannahill e cols17. Sucintamente, os animais sem
qualquer tratamento prévio foram submetidos, sob leve
anestesia com éter sulfúrico (LabSynth. P.A. - A.C.S.), à
administração intracolônica, através de um cateter plástico de
0,8 mm de diâmetro (sonda de aspiração traqueal nº 8
CPL-medical's) marcado aos 8 cm para limitar a distância
da borda anal, de uma solução de ácido acético (LabSynth
. P.A. - A.C.S.) diluído a 7 % e com volume de 3 mL.
Os animais (cinco ratos por gaiola) foram alojados em
ambiente com temperatura e luz controladas, sendo o
fornecimento de ração padrão e água
ad libitum.
Estudaram-se 55 ratos norvérgicos da cepa Wistar,
fornecidos pelo Biotério Central do ICBS/UFRGS/POA
com, pelo menos, 9 semanas de idade, peso não inferior a
180,0 g, com uma média de 276,0 g e desvio padrão de 25,0
g. Ratos com diarréia prévia ao tratamento ou peso
abaixo de 180,0 g foram excluídos. Realizou-se
randomização em blocos para divisão dos animais em quatro grupos:
o grupo da colite induzida (grupo A, n = 15) recebeu
enema de ácido acético a 7% (3 mL) e foi acompanhado
para avaliar-se a evolução da doença; o grupo intervenção
(grupo B, n = 16) foi induzido com ácido acético sendo
tratado com CyA (SANDIMMUN® 100 mg/mL - Sandoz )
na dose de 2,0 mg/kg (0,5 mg = 1 mL) 24 h após a indução
e durante 6 dias consecutivos29 o grupo C ( n = 9)
recebeu CyA na dose de 0,5 mg (1mL) 24 h após um enema
de solução fisiológica e durante 6 dias consecutivos; o
grupo D (n=15) recebeu apenas enema de solução fisiológica
no mesmo volume (3 mL) usado para a indução com
ácido acético. Os grupos C e D foram utilizados para controle.
O experimento estendeu-se por 14 dias. Diariamente
eram avaliados e anotados os pesos dos animais, o consumo
de ração por gaiola, a consistência e o aspecto das fezes.
A partir do 2º dia foram sacrificados (aspiração de
concentrações elevadas de éter sulfúrico), em média, 2
animais do grupo D e 3 animais dos demais grupos. Após
a remoção e abertura longitudinal ao longo da
borda mesentérica procedia-se a lavagem com solução
fisiológica. Os primeiros 14 cm de cólon foram seccionados e
montados em uma placa para exame macroscópico. Para
esta avaliação utilizou-se um estereomicroscópio
(aus-JENA, Alemanha, ocular 6,3 x, regulagem 0,63 a 4x). Após,
foram coletadas três biópsias de cada cólon
escolhendo-se como locais de retirada, as áreas de ulceração e/ou
inflamação e uma área aparentemente íntegra.
Foram colhidas amostras aos 1,0 , 3,0 e 8,0 cm na ausência de
lesões visíveis. Os espécimes eram enrolados e fixados em
solução de formol a 5 % para posterior confecção de
blocos de parafina e preparação de lâminas que foram
coradas por hematoxilina e eosina e avaliadas histologicamente
por microscopia usando-se um microscópio óptico
binocular (Olympus BHZ, Olympus Co. Tóquio, Japão). O
material das biópsias recebeu um tratamento semelhante no que
se refere ao processamento e avaliação histológica.
Os resultados foram avaliados em 4 níveis
verificando-se (1) as variações de peso e ingestão dos animais, (2)
a variação da consistência e aspecto das fezes , (3) as
características macroscópicas e (4) microscópicas da mucosa.
A variação diária de peso foi calculada pela média
da variação dos pesos individuais dos animais em cada
um dos grupos.
Os danos macroscópicos da mucosa foram
avaliados, por dois observadores cegos dos tratamentos, através
de um escore que variava de 0 a 5 tendo sido adaptado
daquele descrito por Morris e cols20 (Tabela 1).
Tabela 1 - Avaliação macroscópica da mucosa
| escore | achados macroscópicos |
| 0 | sem dano |
| 1 | hiperemia localizada SEM ULCERAÇÕES |
| 2 |
ULCERAÇÕES LINEARES sem inflamação significante (pouca hiperemia e sem espessamento da parede) |
| 3 |
ULCERAÇÕES LINEARES com inflamação em UM LOCAL |
| 4 |
DOIS OU MAIS IMPORTANTES locais de inflamação e ulceração ou |
A avaliação microscópica das lâminas das peças e
das biópsias foi realizada por patologista, cego tanto dos
tratamentos quanto da avaliação macroscópica e foi
baseada no Índice Histológico de Atividade da Doença (IHAD)
descrito por Sandborn e cols30 (Tabela 2).
| Tabela 2 - Índice histológico de atividade da doença |
 |
Para a análise estatística utilizaram-se os
programas Stat View 4.02, 1993, Abacus Concepts Inc. e Epi
Info v.6.04, jan/97. Calculou-se a média e o desvio
padrão das variáveis peso, achados macro e microscópicos,
consumo médio por animal/dia e ingestão. Os testes
qui-quadrado e Exato de Fischer foram usados para avaliar
consistência e aspecto das fezes. O Wilcoxon rank test
foi usado nas variáveis peso, ingesta e achados macro e
microscópicos.
Em todos os testes, valores de p £ 0,05 foram
considerados significativos.
RESULTADOS
Para uma melhor adequação às condições técnicas
do laboratório e do biotério, o estudo foi realizado em
quatro etapas. Ao longo destas, houve três mortes: duas no
grupo B e uma no grupo D.
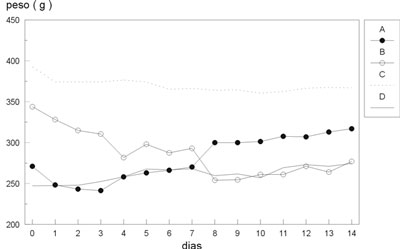
O peso dos animais variou, ao longo do estudo,
entre os diversos grupos. Não houve diferença
estatiscamente significativa entre os grupos A e B enquanto ela foi
significativa entre os grupos C e D. A variação diária do
peso dos animais em cada grupo está apresentada na
figura abaixo (Fig. 1).
 |
|
Fig. 1 - Peso médio diário entre os grupos. |
| * NS, † p = 0, 007 (Wilcoxon rank test) |
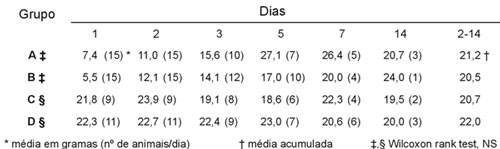
Não se verificaram diferenças estatisticamente
significativas na comparação dos dados de consumo diário
de ração por rato, tanto entre os grupos A e B como C e
D. As variações da ingesta entre os grupos, a partir do
primeiro dia e dos dias subseqüentes em que houve sacrifício
dos animais, estão apresentadas a seguir (Tabela 3).
| Tabela 3 - Variação da ingesta média por animal. |
 |
Em relação a consistência das fezes, não
houve significância estatística quando se compararam os
grupos A e B (qui-quadrado, NS). Já a comparação entre os
grupos C e D foi significativa (Teste Exato de Fischer, p
= 0,007). Estas variações estão expressas na figura que
resume as variações da consistência das fezes nos
diversos grupos (Fig. 2).
Quanto ao aspecto das fezes, os resultados
encontrados não mostraram uma diferença estatística entre os grupos
A e B (qui-quadrado, NS). No entanto, esta diferença
mostrou-se significativa quando se analisaram os grupos C e
D (Teste Exato de Fischer, p = 0,04). A figura a seguir
ilustra estes achados (Fig. 3).
 |
|
|
Fig. 2 - Consistência das fezes nos grupo durante todo o experimento. |
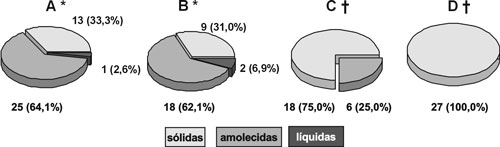 |
| Fig. 3 - Aspecto das fezes nos grupos durante todo o experimento. * qui-quadrado, NS † Teste Exato de Fischer, p = 0,04 |
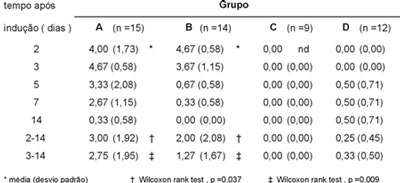
A avaliação macroscópica evidenciou uma
significância estatística (Wilcoxon
rank test) quando se compararam os grupos A e B, tanto no período acumulado do 2º ao 14º
dia quanto do 3º ao 14º dia. Esta estratificação foi feita para
se poder evidenciar, com maior clareza, os efeitos
da ciclosporina no grupo B. A comparação dos grupos C e
D não mostrou significância estatística. Estes resultados
estão apresentados na tabela a seguir (Tabela 4).
| Tabela 4 - Alterações observadas na avaliação macroscópica da mucosa (0 - 5). |
 |
Os aspectos macroscópicos mais significativos das
lesões observadas e classificadas estão demonstrados na
figura a seguir (Fig. 4)
 |
| Fig. 4 - Aspectos macroscópicos relevantes |
Finalmente, foi realizada a avaliação microscópica das lesões nos cólons. A evolução das alterações microscópicas foi estudada através de uma lâmina média para as peças e as biópsias. A comparação dos grupos (Wilcoxon rank test), tanto nas lâminas das peças quanto nas das biópsias, não foi significativa entre os grupos A e B e também entre os grupos C e D mesmo quando estratificados nos períodos do 2º ao 14º e 3º ao 14º dias (Tabela 5).
|
Tabela 5 - Alterações do índice histológico da atividade da doença (0-3) nas peças e biópsias |
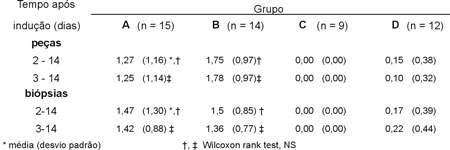 |
O coeficiente de correlação (CC) das médias
acumuladas das lâminas das peças e das biópsias do
índice histológico da atividade da doença (IHAD) foi 0,85
e 0,70, respectivamente para os grupos A e B.
Os aspectos microscópicos mais significativos das
lesões observadas e classificadas são mostrados na figura
a seguir (Fig. 5).
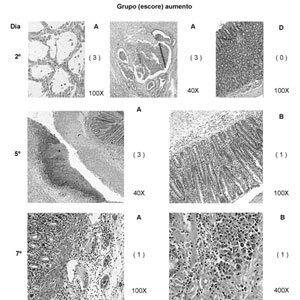 |
| Fig. 5 - Aspectos microscópicos significativos observados nas lâminas das peças no 2º, 5º e 7º dia. |
DISCUSSÃO
As limitações no conhecimento da etiologia da
colite ulcerativa, bem como a inexistência de marcadores
específicos de atividade da doença, dificultam as
intervenções terapêuticas que, desta maneira, concentram-se
principalmente no combate às conseqüências da amplificação
das cascatas imunológica e inflamatória e às
repercussões sistêmicas destas.
A escolha do modelo experimental sempre deve
levar em consideração aquilo a que se propõe o estudo. Assim,
a utilização do modelo de indução de doença aguda pelo
ácido acético está justificada em função da ação
farmaco-dinâmica da CyA que, ao interferir na fase de ativação
das células imunológicas da lâmina própria, principalmente
as células T10,12,25, minimizaria a resposta inflamatória
induzida pelo ácido acético. Além deste aspecto, apesar das
diferenças dos fatores iniciadores da resposta imunológica
em ambas as situações, a colite induzida pelo ácido
acético mostra uma grande semelhança no padrão do
metabolismo do ácido aracdônico verificando-se que, tanto os
produtos da lipo como os da cicloxigenase, são igualmente
dependentes da infiltração neutrocitária seja mediada pelo
ácido acético ou na colite
ulcerativa15,16,18,23,32.
A diversidade e a falta de especificidade de
apresentação das manifestações clínicas, endoscópicas e
histológicas da doença dificulta a criação de um padrão
classificatório reprodutível que seja amplamente aceito e possa ser
utilizado na pesquisa médica. Desta maneira, a introdução
e utilização das variáveis peso, ingesta, consistência e
aspecto das fezes no estudo, teve apenas o intuito de,
ao acompanhar a evolução dos grupos durante o
experimento, observar se os tratamentos produziriam alguma
alteração de interesse.
Ao analisar-se o peso, verifica-se que não houve
diferença significativa entre os grupos A e B apesar da
curva do grupo B ter se mantido descendente por um maior
tempo. Como a perda de peso é consecutiva à cronicidade
da doença ou à intensidade de suas
manifestações33,34, o
próprio método de indução aguda da doença e a rápida
recuperação podem ter sido os responsáveis por estes
achados. A diferença estatisticamente significativa observada
entre os grupos C e D deveu-se, não aos tratamentos mas a
um viés de confusão causado pela grande diferença dos
pesos iniciais em cada um dos grupos. Isto pode ser
explicado uma vez que, como o experimento foi realizado em
etapas e o grupo C foi feito na última etapa, este período de
tempo permitiu aos animais um maior ganho de peso e,
conseqüentemente, a sua diferenciação. No entanto, a
observação das curvas mostrou que, apesar das diferenças
iniciais de peso, não houve variação dos mesmos ao longo do
tempo em função dos tratamentos.
Em relação ao consumo diário de ração pelos
animais, observa-se que também não houve diferenças
significativas tanto entre os grupos A e B como entre os grupos C
e D. Isto fica bem evidenciado ao se cotejar as médias
acumuladas da ingestão diária durante todo o transcorrer
do experimento. Analisando-se as médias de ingestão grupo
a grupo verificou-se que, entre os grupos A e B, a
ascensão destas corresponde exatamente a evolução da doença
aguda aumentando e estabilizando-se a medida que a
doença evoluía favoravelmente. Nos grupos C e D, onde não
houve indução de colite ulcerativa, a ingestão se
manteve inalterada durante todo o tempo de observação.
A avaliação das alterações da consistência e dos
aspecto das fezes apresenta dificuldades já evidenciadas
por Truelove e Witts35. Não se verificaram diferenças
significativas na consistência das fezes nem no seu aspecto,
quando da análise dos grupos A e B. É sabido que nem todos
os casos de colite ulcerativa apresentam alterações
destes parâmetros como ficou bem evidenciado por Both e
cols34 mostrando, exatamente, que muitos pacientes, apesar
de doentes, não apresentavam alterações no padrão de
suas fezes. Lennard-Jones e cols36, em uma revisão de 100
pacientes com proctite, do St. Mark's Hospital,
encontraram 30% de episódios de constipação enquanto 99%
referiam sangue ou muco nas fezes. A aparente
controvérsia quanto à presença de sangue apenas serve para
evidenciar o quanto estes parâmetros podem ser variáveis. As
diferenças, estatisticamente significativas, observadas entre
os grupos C e D tanto na consistência quanto no aspecto
das fezes devem-se, provavelmente, a efeitos adversos da
administração da CyA pela via retal ou à própria variação
na consistência que possivelmente pode ocorrer neste tipo
de animal de experimentação.
A análise dos resultados das alterações
macroscópicas das lesões foi realizada em dois níveis (do 2º-14º e do
3º-14º dia). Esta estratificação teve como objetivo observar a
intensidade dos efeitos da CyA com o transcorrer do
tratamento uma vez que a avaliação do dia 2 quantificava
apenas os efeitos das primeiras 24 h da mesma sobre a
mucosa. Em ambas as situações verificou-se uma diferença
estatisticamente significativa na comparação entre os grupos A e
B. Estes achados evidenciaram que a CyA, na dose
utilizada (2,0 mg/kg), conseguiu apresentar um resultado positivo
abreviando a evolução da doença. O uso da via retal para
a administração de CyA, nos casos de colite esquerda e
distal, refratários aos tratamentos clássicos tem sido advogado
já há algum tempo. A justificativa para a utilização desta
via reside, principalmente em dois aspectos: um deles, a
estreita janela terapêutica da CyA quando usada pelas vias oral
e intravenosa e o outro, exatamente por prevenir esta
toxicidade ao proporcionar baixas concentrações
séricas37. Isto decorre do fato de que a administração de enemas na forma
aquosa não só previne a sua absorção como também permite
um tempo de contato mais prolongado do fármaco com a
mucosa proporcionando níveis teciduais colônicos até dez
vezes maiores do que aqueles observados quando da utilização
da via oral e comparáveis com os obtidos pela via IV sem
os riscos das altas concentrações plasmáticas da
droga10,12,28. Resultados semelhantes aos observados no presente
estudo foram obtidos por Murthy e
cols29 em um trabalho experimental que utilizou o sulfato de dextram para indução
da colite. Em recente revisão da literatura internacional,
não foram encontradas publicações testando a associação
de indução de colite ulcerativa aguda por ácido acético e o
tratamento com enemas de CyA. Estudos abertos30,31
observaram resultados positivos em mais de 50% dos pacientes
tratados com enemas existindo relatos de uma correlação
entre o tempo de retenção do enema e uma resposta
positiva ao tratamento11.
Na comparação dos grupos C e D não se
evidenciou nenhuma alteração significativa demonstrando, portanto,
que a administração de enemas de CyA em mucosa normal
não produz alterações dignas de nota. Os subsídios para
esta afirmação são encontrados naquela constatação de que
a utilização desta via de administração proporcionava
níveis teciduais colônicos elevados sem contudo apresentar
aumentos importantes nos níveis plasmáticos da
CyA10,12.
A estratificação da avaliação microscópica dos
efeitos da CyA sobre a mucosa, tanto nas lâminas das peças
como nas das biópsias, foi realizada da mesma maneira que
para a avaliação macroscópica e atendeu aos mesmos
propósitos desta. Comparando-se os resultados obtidos nos
grupos A e B, tanto nas lâminas das peças como nas
das biópsias, não se observaram diferenças significativas o
que se contrapõe aos achados macroscópicos nos mesmos
grupos e nas mesmas condições de análise.
A literatura a respeito da colite ulcerativa é rica
em citações sobre o descompasso entre os
achados macroscópicos e histológicos como foi demonstrado
por Spiliadis CA e Lennard-Jones38. Da mesma forma,
existem dificuldades no estabelecimento de
padrões histológicos de comparação válidos e reprodutíveis
como ficou bem demonstrado se forem comparados os
índices histológicos propostos por Sandborn e
cols30 , Powell-Tuck e
cols39 e Gomes e cols40. Em
nenhum momento, qualquer destes índices contempla um
critério para o processo de regeneração da mucosa.
Quando da avaliação microscópica, o patologista ressentiu-se
da falta deste critério o que o obrigava a pontuar uma
lesão, com francas características regenerativas,
como uma lesão grave na medida em que não havia
aquela possibilidade no índice utilizado. Este, por não
possibilitar uma avaliação mais precisa da eficácia da
CyA, tenha talvez constituído um importante viés durante
a avaliação microscópica das lesões podendo, assim,
explicar a aparente discrepância entre os resultados
das avaliações macro e microscópicas.
Do mesmo modo, a ausência de diferença entre
os grupos C e D, mesmo consideradas aquelas
dificuldades de padronização de índices, pode ser
convenientemente explicada pelas mesmas razões discutidas
anteriormente onde ficou demonstrado que a CyA, em mucosa
íntegra, não era capaz de produzir alterações relevantes.
É importante ressaltar que os resultados da
avaliação microscópica, tanto nas lâminas das peças como nas
das biópsias, mostraram um alto índice de correlação tanto
para o grupo A quanto para o grupo B apresentando uma
aplicação clínica importante se considerado o grau de
fidedignidade que a análise das biópsias possa propiciar.
A partir dos resultados obtidos, o presente estudo
permite concluir que o método de indução de colite
ulcerativa pela utilização de ácido acético a 7% é efetivo e factível
e que o emprego de CyA, na dose de 2,0 mg/kg (0,5
mg) mostrou ser eficiente quando se consideraram os
aspectos macroscópicos da mucosa colônica o que é compatível
com os dados de literatura disponíveis. Outros estudos são
necessários para se avaliar os aspectos pertinentes a esta
via de administração e a utilização da CyA como uma
opção segura e correta no tratamento da colite ulcerativa.
Abstract: Research on alternative drugs to treat ulcerative colitis is very important considering its increase on
incidence,
peaking on youth. Target issues have been mainly focusing on progress in the understanding of multiple etiopathogenic mechanisms and
severe side effects as well as failure of conventional therapies.
Therefore, to test the efficacy of cyclosporine A (CyA) enemas on the treatment of ulcerative colitis
and, at the same time, develop
an experimental model of colitis induction in rats with dilute acetic acid a
randomized, single-blinded placebo-controlled trial was conducted.
Ulcerative colitis was experimentally induced in 55 adult male Wistar rats using a 7% acetic acid solution by rectal
infusion. The
rats were induced with acetic acid solution alone (group A, n=15) and further treated with CyA (2
mg/Kg/day) enemas (group B,
n=16), infused with saline solution and treated with CyA or saline solution
alone; group C (n=9) and D (n=15), respectively. During the
experiment (14 days) samples of each group were sacrificed on day 2, 3, 4, 5, 7 and 14 to determine macro and microscopic disease activity
scores. Daily variations on weight, food intake and stool characteristics were also
observed, but no significant differences were found for
these features for any group. Histologically, groups A and B were graded an average score of 1,27 and 1,75, respectively
(NS). However, macroscopic appearance of disease activity was significantly improved either from day 2 to 14 or from day 3 to 14 in rats treated
with CyA (group B) as compared to those (group A) without treatment (Wilcoxon rank
test, p=0.037 and p=0.009).
In conclusion, CyA given by rectal enema is safe since no changes in
weight, intake or stools were observed, and CyA at a dose of 2 mg/kg/day was effective to improve
outcome. The model of colitis induction is suitable and cost-effective.
Keywords: Ulcerative colitis, experimental, cyclosporine
REFERÊNCIAS BIBLIOGRÁFICAS:
1. Hodgson HJ.The natural history of treated ulcerative colitis
[editorial; comment]. Gastroenterology 1994;107:300-2.
2. Teixeira MG, Brunetti Netto C, Rosoky RM, Habr-Gama A, Pinotti
HW. Manifestações extra-intestinais da retocolite ulcerativa.
Rev bras Coloproct 1988;8:45-49.
3. Houli J, Netto GM. Retocolite ulcerativa inespecífica.
Rev bras Coloproct 1984;4:191-205.
4. Hay JW, Hay AR. Inflammatory Bowel Disease: costs-of-illness.
J Clin Gastroenterol 1992;14:309-17.
5. Pinczowski D, Ekbom A, Baron J, Yuen Jet, Adami HO. Risk Factors
for colorectal cancer in patients with ulcerative colitis: a case control
study. Gastroenterology 1994;107:117-20.
6. Broström O, Löfberg R, Nordenwall B, Öst Ã, Hellers G. The risk
of colorectal cancer in ulcerative colitis: an epidemiological study.
Scand J Gastroenterol 1987;22:1193-99.
7. Lennard-Jones JE, Melville DM, Morson BC, Ritchie JK, Williams
CB. Precancer and cancer in extensive ulcerative colitis: findings among
401 patients over 22 years. Gut 1990;31:800-06.
8. Ekbom A, Helmick C, Zack M, Adami HO. Ulcerative colitis and
colorectal cancer. A population-based study. N Engl J
Med 1990;323:1228-33.
9. Ferguson A, Sedgwick DM, Drummond J. Morbidity of juvenile
onset inflammatory bowel disease: effects on education and employment in
early adult life. Gut 1994;35:665-68
10. Berstein CN, Shanahan F. Immunomodulatory therapy in
inflammatory bowel disease. In: Targan RS, Shanahan F. Eds. Inflammatory
bowel disease: from bench to bedside. Baltimore; Williams &
Wilkins,1994;503-523.
11. Van Hogezand RA. Medical management of patients with
difficult-to-treat inflammatory bowel disease. Neth J
Med 1994;45:55-59.
12. Brynskov J. Cyclosporin for inflammatory bowel disease:
mechanisms and possible actions. Scand J
Gastroenterol 1993;28:849-57.
13. Fuchs FD, Wannmacher L. Métodos de investigação
farmacológico-clínica. in: Fuchs FD & Wannmacher Eds. Farmacologia Clínica. 2ed. Rio
de Janeiro;Guanabara Koogan SA,1998,7-16.
14. MacPherson BR & Pfeiffer CJ.Experimental production of diffuse colitis
in rats. Digestion 1978;17:135-170.
15. Fedorak RN, Empey LR, MacArthur C, Jewell LD. Misoprostol provides
a colonic mucosal protective effect during acetic acid-induced colitis
in rats. Gastroenterology 1990;98:615-25.
16. Yamada T, Fujinamoto K, Tso P, Fujinamoto T, Gaginella TS, Grislam
MB. Misoprostol accelerates colonic mucosal repair in acetic acid
induced colitis. J Pharmacol Exp Ther 1992;260:313-18.
17. Tannahill CL, Stevenot SA, Campbell-Thompson M, Nick HS,
Valentine JF. Induction and immunolocalization of manganese superoxide
dismutase in acute acid-induced colitis in the rat.
Gastroenterology 1995;109:800-811.
18. Fabia R, Ar'Rajab A, Willén R, et al. Effects of phosphatidylcholine
and phosphaticylinositol on acetic-acid-induced colitis in the rat.
Digestion 1992;53:35-44.
19. Zahavi I, Burg Z, Marcus H, Karmeli F, Nusinovitz M, Dinari G.
Therapeutic effect of colloid bismuth subcitrate in experimental colitis in the
rat. Digestion 1995;56:211-13.
20. Morris GP, Beck PL, Herridge MS, Depew WT, Szewczuk MR,
Wallance JL. Hapten-induced model of chronic inflammation and ulceration in
the rat colon. Gastroenterology 1989;96:795-803.
21. Stenson WF. Animals models of inflammatory bowel disease. In:
Targan RS, Shanahan F. Inflammatory bowel disease: from bench to
bedside. Baltimore:Williams & Wilkins,1994;180-192.
22. Warren BF, Watkins PE. Animals models of inflammatory bowel disease.
J Pathol 1994;172:313-16.
23. Fabia R, Ar'Rajab A, Willén R, Andersson R, Bengmark S. Effect of
putative phospholipase A2 inhibitors on acetic acid-induced acute colitis in
the rat. Br J Surg 1993;80:1199-1204.
24. Borel JF, Feurer C, Gubler HU, Stähelin H. Biological effects of
cyclosporin A: a new antilymphocytic agent. Agents
Actions 1976;6:468-75.
25. Linn FV, Peppercorn MA. Drug therapy for inflammatory bowel
disease: part II. Am J Surg 1992;164:178-85.
26. Sandborn WJ. Cyclosporine therapy for inflammatory bowel
disease: definitive answers and remaining questions.
Gastroenterology 1995;109:1001-03.
27. Treem WR, Hyams JS. Cyclosporine therapy for gastrointestinal
disease. J Pediatr Gastroenterol Nutr 1994;18:270-78.
28. Present DH. Cyclosporine and other immunosupressive agents:
current and future role in the treatment of inflammatory bowel disease.
Am J Gastroenterol 1993;88:627-30.
29. Murthy SNS, Cooper HS, Shim H, Sholi RS, Braulin SA, Sedergron
DJ. Treatment of dextran sulfate sodium-induced murine colitis by
intracolonic cyclosporin. Dig Dis Sci 1993;38:1722-34.
30. Sandborn WJ. Tremaine WJ, Schroeder KW, Steiner BL. Batts KP,
Lawson GM. Cyclosporine enemas for treatment-resistant, mildly to
moderately active, left-sided ulcerative colitis.
Am J Gastroenterol 1993;88:640-45.
31. Winter TA, Dalton HR, Merrett MN, Campbell A, Jewell DP.
Cyclosporine A retention enemas in refractory distal ulcerative colitis and
pouchits. Scand J Gastroenterol 1993;28:701-04.
32. Empey LR, Jewell LD, Manohar L, Fedorak RN, et al. Fish oil-enriched
diet is mucosal protective against acetic-induced colitis in rats.
Can J Physiol Pharmacol 1991;69:480-87.
33. Leijonmarck CE, Persson PG, Hellers G. Factors affecting colectomy
rate in ulcerative colitis: an epidemiologic study.
Gut 1990;31:329-33.
34. Both H, Torp-Pedersen K, Kreiner S, Hendriksen C, Binder V.
Clinical appearance at diagnosis of ulcerative colitis and Crohn's disease in
a regional patient group. Scand J
Gastroenterol 1983;18:987-91.
35. Truelove SC, Witts LJ. Cortisone in ulcerative colitis. Final report on
a therapeutic trial. Br Med J 1955;2:1041-48.
36. Lennard-Jones JE, Cooper GW, Newell AC, Wilson CWE, Avery Jones
F. Observations on idiopathic proctitis.
Gut 1962;3:201-06.
37. Sartor RB. Cyclosporine therapy for inflammatory bowel disease.
N Engl J Med 1994;330:1897-98.
38. Spiliadis CA, Lennard-Jones JE. Ulcerative colitis with relative sparing
of the rectum. Clinical features, histology, and prognosis.
Dis Colon Rectum 1987;30:334-36.
39. Powell-Tuck J, Day DW, Buckell NA, Wadsworth J, Lennard-Jones
JE. Correlations between defined sigmoidoscopic appearances and
other measures of disease activity in ulcerative colitis.
Dig Dis Sci 1982;27:533-37.
40. Gomes P, du Boulay C, Smith CL, Holdstock G. Relationship
between disease activity indices and colonoscopic findings in patients wity
colonic inflammatory bowell disease. Gut 1986;27:92-95.
Endereço para correspondência:
Roberto Amaral
Av. Mostardeiro 157, sala 305
Bairro Moinhos de Vento
Porto Alegre RS
CEP: 90430-001
Fone 0(xx) 51 33467855
Trabalho realizado e apresentado como dissertação na Faculdade de Medicina da UFRGS CPGC para obtenção do título de mestre em Medicina: Cirurgia - Porto Alegre, RS.