ARTIGOS ORIGINAIS
VALOR DA DOSAGEM DO ANTÍGENO CARCINOEMBRIONÁRIO, DA FOSFATASE ALCALINA E DA GAMA-GLUTAMIL TRANSPEPTIDASE NO SEGUIMENTO DE PACIENTES COM CÂNCER DE CÓLON E DE RETO
SANDRA PEDROSO DE MORAES - TSBCP
ARNALDO AMSTALDEN NETO
FELIPE LONGO SANCHES
FLÁVIO ANTONIO QUILICI - TSBCP
MORAES SP; AMSTALDEN NETO A; SANCHES FL; QUILICI FA. Valor da dosagem do antígeno carcinoembrionário, da fosfatase
alcalina e da gama-glutamil transpeptidase no seguimento de pacientes com câncer de cólon e de reto.
Rev bras Coloproct, 2003;23(3):163-167
RESUMO: Os marcadores biológicos representam os exames de primeira linha na investigação das recidivas neoplásicas. No
câncer colorretal, a relação custo-benefício da realização simultânea das dosagens séricas de CEA, fosfatase alcalina (FA) e
gama-glutamil-transpeptidase ( GT) e a validade de se continuar dosando CEA, quando o exame inicial é normal, não estão claras na
literatura. Com o objetivo de estudar o comportamento desses marcadores na evolução dos tumores colorretais, foram estudados 100
pacientes, acompanhados no PO por tempo médio de 30 meses, no período de janeiro de 1991 a fevereiro de 1999 (8 anos). Cinqüenta e
três eram do sexo masculino e quarenta e sete do feminino, com idade média de 60 anos. Todos os pacientes foram submetidos a
tratamento cirúrgico, sendo que 12 já apresentavam metástases e 17 apresentaram recidiva durante o seguimento. Os resultados
mostraram sensibilidade e especificidade de CEA, FA e
GT) e a validade de se continuar dosando CEA, quando o exame inicial é normal, não estão claras na
literatura. Com o objetivo de estudar o comportamento desses marcadores na evolução dos tumores colorretais, foram estudados 100
pacientes, acompanhados no PO por tempo médio de 30 meses, no período de janeiro de 1991 a fevereiro de 1999 (8 anos). Cinqüenta e
três eram do sexo masculino e quarenta e sete do feminino, com idade média de 60 anos. Todos os pacientes foram submetidos a
tratamento cirúrgico, sendo que 12 já apresentavam metástases e 17 apresentaram recidiva durante o seguimento. Os resultados
mostraram sensibilidade e especificidade de CEA, FA e  GT em detectar metástases na operação de, respectivamente, 75%; 64%; 25%;
93%; 36%; 86% e em recidivas de 93%; 98%; 36%; 76%; 42%; 80%, respectivamente. O CEA quase sempre se elevou meses antes
que FA e
GT em detectar metástases na operação de, respectivamente, 75%; 64%; 25%;
93%; 36%; 86% e em recidivas de 93%; 98%; 36%; 76%; 42%; 80%, respectivamente. O CEA quase sempre se elevou meses antes
que FA e  -GT, exceto em um paciente com metástases e noutro com recidiva. Dos pacientes que apresentaram metástases ou
recidivas 45,9% tinham CEA inicial aumentado e somente 19,2% tinham CEA normal. Todos os pacientes que apresentaram CEA normal
no Pré-OP, tiveram elevação desse marcador quando se diagnosticou a recidiva, exceto no paciente nº 12. Concluiu-se que não
há benefício na dosagem da FA e da dGT para diagnóstico de metástases hepáticas e que o CEA deve fazer parte do rastreamento
de metástases, mesmo quando o seu valor inicial for normal.
-GT, exceto em um paciente com metástases e noutro com recidiva. Dos pacientes que apresentaram metástases ou
recidivas 45,9% tinham CEA inicial aumentado e somente 19,2% tinham CEA normal. Todos os pacientes que apresentaram CEA normal
no Pré-OP, tiveram elevação desse marcador quando se diagnosticou a recidiva, exceto no paciente nº 12. Concluiu-se que não
há benefício na dosagem da FA e da dGT para diagnóstico de metástases hepáticas e que o CEA deve fazer parte do rastreamento
de metástases, mesmo quando o seu valor inicial for normal.
Unitermos: antígeno carcinoembrionário, fosfatase alcalina, gama-glutamiltransferase
INTRODUÇÃO
A incidência do câncer colorretal vem
apresentando um aumento consistente ao longo das
últimas décadas. O Instituto Nacional do Câncer fez
previsão de mais 19.000 novos casos para o ano de
20021.
Graças ao avanço no seu diagnóstico e em
sua terapêutica, o número de pacientes acompanhados
no período pós-operatório (PO) vem também
aumentando progressivamente. Os exames indicados para
o rastreamento de sua recidiva devem ter qualidade
para detectar metástases e/ou recidivas precoces e com
custo acessível para o Sistema de Saúde Nacional. Não
se justifica a associação de testes cujos resultados se
sobrepõem, ou seja, só acrescentam custos, sem
trazer benefícios aos pacientes.
Há autores que afirmam que dosagens
de fosfatase alcalina (FA) e
gama-Glutamil-transpeptidase ( -GT) contribuem para seu estadiamento e/ou
acompanhamento dos enfermos submetidos à
operação colorretal por enfermidades
malígnas2,3,4 e vários
serviços médicos no nosso meio têm utilizado,
rotineiramente, esses exames para detecção de metástases
hepáticas e para o acompanhamento PO. No entanto,
algumas publicações afirmam que as dosagens
dessas enzimas não contribuem para o diagnóstico das
recidivas dos tumores colorretais.5,6
-GT) contribuem para seu estadiamento e/ou
acompanhamento dos enfermos submetidos à
operação colorretal por enfermidades
malígnas2,3,4 e vários
serviços médicos no nosso meio têm utilizado,
rotineiramente, esses exames para detecção de metástases
hepáticas e para o acompanhamento PO. No entanto,
algumas publicações afirmam que as dosagens
dessas enzimas não contribuem para o diagnóstico das
recidivas dos tumores colorretais.5,6
O antígeno carcinoembrionário (CEA),
embora não tenha valor no rastreamento populacional de
indivíduos com tumores colorretais, é útil no seu
acompanhamento pós-operatório e a elevação de sua dosagem
no PO, poderá indicar a presença da recidiva tumoral e
orientar a solicitação de exames mais sofisticados para
confirmar esse diagnóstico e para localizar essa
recidiva.7,8
Há indícios de que pacientes que
apresentam CEA normal no período pré-operatório (Pré-OP)
seriam portadores de neoplasias "escassamente
produtoras desse antígeno"
9, e manteriam valores baixos de CEA no acompanhamento PO, tornando inútil o
seu uso no rastreamento das recidivas.
Este trabalho teve como objetivos avaliar:
1) Se a FA e o  -GT adicionam dados ao CEA
sérico, que poderiam contribuir para o diagnóstico mais
precoce de recidivas dos tumores colorretais, e
-GT adicionam dados ao CEA
sérico, que poderiam contribuir para o diagnóstico mais
precoce de recidivas dos tumores colorretais, e
2) Se, com a dosagem normal de CEA sérico no
pré-operatório, o mesmo teria valor no seguimento
de pacientes com câncer de cólon e reto.
PACIENTES E MÉTODOS
Foram avaliados 100 pacientes operados no Serviço de Coloproctologia do Hospital
Universitário Celso Pierro da PUC Campinas, entre janeiro de
1991 a fevereiro de 1999 (oito anos). Destes, 53 eram
do sexo masculino e 47 do feminino, com idade
variável entre 19 e 94 anos (média de 60 anos). Todos
eram portadores de adenocarcinomas colorretais e
foram submetidos a tratamento cirúrgico. Os tumores
estavam localizados em reto e sigmóide em 72
pacientes (72%) e em cólon em 26 (26%). Apresentaram
tumores sincrônicos 2 pacientes (2%).
O tempo médio de acompanhamento PO
foi de 30 meses. Todos realizaram dosagens séricas
de CEA, FA e  -GT no período pré-operatório e no
PO aos 30, 90, 180, 270, 360 dias do 1º ano. No 2º ano,
de 6/6 meses e anualmente a seguir. Os valores
considerados normais foram CEA
-GT no período pré-operatório e no
PO aos 30, 90, 180, 270, 360 dias do 1º ano. No 2º ano,
de 6/6 meses e anualmente a seguir. Os valores
considerados normais foram CEA  5 ng/ml, FA
5 ng/ml, FA  240 U/L,
240 U/L,  -GT
-GT  32 U/L.
32 U/L.
No ato operatório foram detectadas
metástases em 12 pacientes (12%) e no PO 17 enfermos
(17%) apresentaram recidivas (metástases hepáticas
e/ou carcinomatose peritoneal) durante seguimento.
RESULTADOS
A sensibilidade e a especificidade dos
exames laboratoriais para detectar metástases na data das
operações e das recidivas encontram-se na Tabela-1.
|

|
| Tabela 1 - Sensibilidade (S) e especificidade (E) dos
exames laboratoriais para detectar metástases na data das
operações (O) e das recidivas (R). |
Os valores de CEA, FA e  -GT, obtidos das mesmas coletas de sangue, no Pré e no PO dos
pacientes com metástases, foram transformados em
percentagem de elevação, considerando-se o valor
máximo da normalidade do exame como 100%. Esses
dados encontram-se na Tabela-2.
-GT, obtidos das mesmas coletas de sangue, no Pré e no PO dos
pacientes com metástases, foram transformados em
percentagem de elevação, considerando-se o valor
máximo da normalidade do exame como 100%. Esses
dados encontram-se na Tabela-2.
|
|
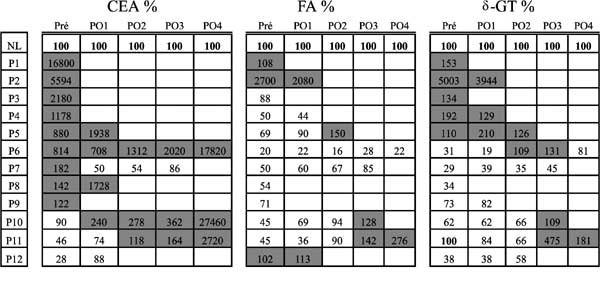
| Tabela 2 - Porcentagem de elevação de alguns valores dos exames laboratoriais dos pacientes (P) que
apresentaram metástases, considerando-se o valor máximo da normalidade como 100%, nos períodos pré-operatório (Pré) e
pós-operatório (PO), coletados em data correspondente.
|
O mesmo foi realizado para os pacientes
que apresentaram recidivas, incluindo-se as
percentagens calculadas nas datas das recidivas tumorais (Tabela-3).
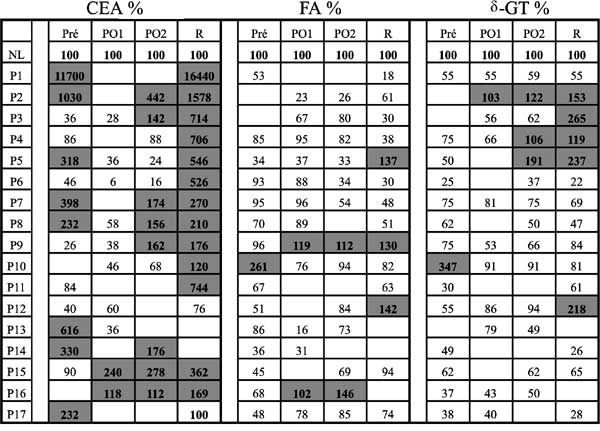 |
| Tabela 3 - Porcentagem de elevação dos valores dos exames laboratoriais dos pacientes (P) que apresentaram
recidivas, considerando-se o valor máximo da normalidade como 100%, nos períodos pré-operatório (Pré), pós-operatório (PO) e
nas datas de recidivas (R), coletados em data correspondente.
|
Para facilitar a visibilização global dos
dados alterados nas tabelas, os valores máximos da
normalidade foram colocados com "números em negrito" e
os valores acima da normalidade foram colocados em "células escuras".
Em janeiro de 2003, o Sistema Único de
Saúde (SUS) repassava aos hospitais os seguintes
valores pela realização dos exames laboratoriais: CEA -
R$ 13,35 = US$ 3,7; FA - R$ 2,01 = US$ 0,56 e  -GT - R$ 3,51 = US$ 0,98.
-GT - R$ 3,51 = US$ 0,98.
DISCUSSÃO
Tabagismo e várias moléstias, que não os
carcinomas colorretais, podem elevar os valores do
CEA e resultar em falso positivo, tais como pancreatite,
cirrose hepática, úlcera péptica, retocolite
ulcerativa, uremia e neoplasias de outra origem. Bem como,
percentagem significante de pacientes com
câncer colorretal localizado na mucosa ou na submucosa
também apresentam CEA normal. Não se justifica o
uso de CEA como técnica de rastreamento
populacional para a neoplasia maligna
colorretal.10
A elevação de CEA no Pré-OP pode
ocorrer tanto pela extensão local da neoplasia como pela
presença de metástases. A Tabela-1 deste trabalho
mostrou que a sensibilidade do CEA foi de 75% e que
a sua especificidade para detectar metástases foi
baixa (64%). Portanto a dosagem de CEA só é útil para
o seguimento PO dos pacientes submetidos a
tratamento cirúrgico, com intenção curativa, de neoplasia
maligna colorretal.
No acompanhamento, na suspeita de
metástases hepáticas, a elevação de CEA ocorreu com
freqüência muito maior que as enzimas
hepáticas.5 Nenhum outro marcador sérico, ou mesmo a
combinação de marcadores, foi superior ao CEA no diagnóstico
da recidiva de tumores colorretais6. Na
literatura5,11,12, assim como neste trabalho, a sensibilidade da  -GT foi discretamente maior que a da FA; no entanto,
ambas foram, no geral, muito baixas. Suas
especificidades, apesar de elevadas, não apresentaram vantagens,
visto que, nas datas em que os exames foram realizados,
as metástases já haviam sido detectadas por exame
de imagens ou até mesmo pelo exame físico.
-GT foi discretamente maior que a da FA; no entanto,
ambas foram, no geral, muito baixas. Suas
especificidades, apesar de elevadas, não apresentaram vantagens,
visto que, nas datas em que os exames foram realizados,
as metástases já haviam sido detectadas por exame
de imagens ou até mesmo pelo exame físico.
Avaliando-se as Tabelas 2 e 3, verificou-se
que o CEA quase sempre se elevou meses antes da
elevação de FA e  -GT. Quando estes últimos se
elevaram, geralmente o CEA já apresentava valores dez
vezes maiores que o limite superior da normalidade.
-GT. Quando estes últimos se
elevaram, geralmente o CEA já apresentava valores dez
vezes maiores que o limite superior da normalidade.
Somente dois pacientes com metástases
não apresentaram elevação de CEA. O primeiro (nº 12
da Tabela-2), apresentou elevação muito discreta, só
de FA no Pré-OP e o segundo (nº 12 da Tabela-3)
apresentou elevação maior, de FA e  -GT, quando foram detectadas metástases hepáticas no
acompanhamento PO. No primeiro paciente, as metástases
foram diagnosticadas por exame de ultrassom e
confirmadas no intra-operatório, portanto o único paciente que
foi beneficiado pelo exame de FA e
-GT, quando foram detectadas metástases hepáticas no
acompanhamento PO. No primeiro paciente, as metástases
foram diagnosticadas por exame de ultrassom e
confirmadas no intra-operatório, portanto o único paciente que
foi beneficiado pelo exame de FA e  -G foi segundo paciente (nº 12 da Tabela-3) ou seja 1% do total de
pacientes, menor que a freqüência encontrada na
literatura, que foi de 2,2%5.
-G foi segundo paciente (nº 12 da Tabela-3) ou seja 1% do total de
pacientes, menor que a freqüência encontrada na
literatura, que foi de 2,2%5.
Segundo Rocklin e cols.5, a exclusão do
acompanhamento PO com o FA e o  -GT nos Estados Unidos, resultaria em economia de US$ 28.000.000.
No Brasil, a solicitação PO desses dois exames
causaram um aumento de 42,3% nos custos laboratoriais
com marcadores, recursos que poderiam ser aplicados
em melhorias da qualidade de aparelhos para
diagnóstico por imagem.
-GT nos Estados Unidos, resultaria em economia de US$ 28.000.000.
No Brasil, a solicitação PO desses dois exames
causaram um aumento de 42,3% nos custos laboratoriais
com marcadores, recursos que poderiam ser aplicados
em melhorias da qualidade de aparelhos para
diagnóstico por imagem.
Como a elevação de CEA Pré-OP foi
maior nos pacientes com neoplasia mais avançada, de
acordo com a classificação de Dukes ou com a fixação
por contigüidade,13 a presença de CEA inicial elevado
é sinal de mau prognóstico. Estatisticamente
é significante a relação dos níveis de CEA elevado
com a presença de
recidiva.7,9,10,12,13,14,15 Sua elevação
não trouxe informações que permitissem selecionar a
terapêutica, mas serve de alerta para o risco de
recidiva15,16. Neste trabalho apresentaram metástases ou
recidivas 45,9% dos pacientes com CEA inicial (Pré-OP)
aumentado e somente 19,2% dos enfermos com CEA
Pré-OP normal, excluindo-se os 11 pacientes que tiveram
extraviados seu valor de CEA inicial.
Os pacientes submetidos à operação com
intenção curativa apresentaram níveis de CEA mais
baixos em torno de 3 a 4 semanas do período
pós-operatório.7 Nos pacientes deste trabalho a 1ª coleta de
sangue para dosagens dos marcadores no PO foi feita
nesse período.
Há relatos de que o carcinoma colorretal
escassamente produtor de CEA, ou seja, com nível
sérico baixo desse antígeno, não teria nele um bom
marcador para acompanhamento PO9. Mas
Corman13 relatou que 44% dos pacientes com CEA normal no Pré-OP
apresentaram CEA elevado quando foram detectadas
recidivas. Todos os pacientes deste trabalho, que
apresentaram CEA normal no Pré-OP, tiveram elevação
desse marcador quando se diagnosticou a recidiva, em
geral, entre 12 e 24 meses após o ato operatório, exceto
o paciente nº 12.
A Sociedade Americana de Oncologia
Clínica16, após amplo estudo da literatura, estabeleceu
o "colorectal cancer surveillance
guidelines" que recomenda o uso exclusivo do CEA, como exame
laboratorial, no rastreamento de neoplasia colorretal.
Portanto, de acordo com os resultados
obtidos neste trabalho retrospectivo, pode-se concluir que a
dosagem sérica de FA e  -GT não deve ser usada
rotineiramente para o diagnóstico e acompanhamento
pós-operatório de pacientes com câncer de cólon e reto e que o CEA
sempre deverá fazer parte dos exames de rastreamento de
recidivas PO do câncer colorretal, mesmo quando seus
valores iniciais (Pre-OP) estejam normais.
-GT não deve ser usada
rotineiramente para o diagnóstico e acompanhamento
pós-operatório de pacientes com câncer de cólon e reto e que o CEA
sempre deverá fazer parte dos exames de rastreamento de
recidivas PO do câncer colorretal, mesmo quando seus
valores iniciais (Pre-OP) estejam normais.
SUMMARY: Prognostic markers are first choice tests to investigate metastatic relapses. In colorectal cancer the
cost-effectiveness ratio of carcinoembryonic antigen (CEA), alkaline Phosphatase (FA) and gamma-glutamyl-transpeptidase ( GT) and the value of performing ongoing tests of CEA level after normal initial tests remain unclear in the literature. One hundred patients were
followed up to study these markers in the outcome of colorectal tumors. Mean post-operative follow up was 30 months from January
1991 through February 1999 (08) years. Fifty-three patients were male and forty-seven were female, mean age was 60 years . All
patients had undergone surgery, twelve already had metastasis and 17 relapsed during the follow up. The results found CEA, FA and
?-GT sensitivity in detecting metastasis during surgery, and they were respectively as follows; 75%, 64%; 25%; 93%; 36%; 86% and
in relapses they were 93%; 98%; 36%; 76%; 42%; 80%, respectively. Almost always CEA, FA and
GT) and the value of performing ongoing tests of CEA level after normal initial tests remain unclear in the literature. One hundred patients were
followed up to study these markers in the outcome of colorectal tumors. Mean post-operative follow up was 30 months from January
1991 through February 1999 (08) years. Fifty-three patients were male and forty-seven were female, mean age was 60 years . All
patients had undergone surgery, twelve already had metastasis and 17 relapsed during the follow up. The results found CEA, FA and
?-GT sensitivity in detecting metastasis during surgery, and they were respectively as follows; 75%, 64%; 25%; 93%; 36%; 86% and
in relapses they were 93%; 98%; 36%; 76%; 42%; 80%, respectively. Almost always CEA, FA and  -GT were increased some months earlier, except for one patient with metastasis and another one that relapsed, 45.9% of the patients had increased initial CEA
and only 19.2% had normal CEA. All patients with normal CEA in the post-operative had an increase of this marker if relapse
was diagnosed, except for patient No. 12. In conclusion, FA and
-GT were increased some months earlier, except for one patient with metastasis and another one that relapsed, 45.9% of the patients had increased initial CEA
and only 19.2% had normal CEA. All patients with normal CEA in the post-operative had an increase of this marker if relapse
was diagnosed, except for patient No. 12. In conclusion, FA and  GT do not provide any benefits to diagnose metastatic liver cancer
and CEA should be included in metastatic screening tests even if its initial level is normal.
GT do not provide any benefits to diagnose metastatic liver cancer
and CEA should be included in metastatic screening tests even if its initial level is normal.
Key words: carcinoembryonic antigen, alkaline phosphatase, gamma-glutamyltransferase
Referências Biliográficas
1 Estimativa da incidência e mortalidade por câncer no
Brasil. Disponível em: <
http://www.inca.gov.br/cancer/epidemiologia/estimativa2002/sintese.html >. Acesso em: 19 nov.2002.
2 Klompje J, Petrelli NJ, Herrera L & Mittelman A.
The prognostic value of alkaline phosphatase for resection
of solitary liver metastasis from colorectal carcinoma.
Eur J Surg Oncol; 13: 345-7, 1987.
3 Cooper EH, Turner R, Steele L, Neville AM & Mackay
AM. The contribution of serum enzymes and
carcinoembryonic antigen to the early diagnosis of metastatic colorectal
cancer. Br J Cancer; 31: 111-7, 1975.
4 Almersjö O, Bengmark S & Hafström Lo. Liver
metastases found by follow-up of patients operated on for
colorectal cancer. Cancer; 37: 1454-7, 1976
5 Rocklin MS, Senagore AJ & Talbott TM. Role
of carcinoembryonic antigen and liver function tests in
the detection of recurrent colorectal carcinoma.
Dis Colon Rectum; 34: 794-7, 1991.
6 Northover J. The use of prognostic markers in surgery
for colorectal cancer. Eur J Cancer; 31A:1207, 1995.
7 Engaras B, Kewenter J, Nilsson O, Wedel H & Hafström
L. CEA, CA 50 and CA 242 in patients surviving
colorectal cancer without recurrent disease.
EJSO; 27: 43-8, 2001.
8 Beck PR, Belfield A, Spooner RJ, Blumgart LH & Wood
CB. Serum enzymes in colorectal cancer.
Cancer; 43:1772-6, 1979.
9 Waisberg J, Landman G, Cha ASH, Henriques AC, Gaspar
HA & Speranzini MB. Padrão da distribuição tecidual do CEA
no carcinoma colo-retal: relação com o nível sérico do CEA
e classificação de Dukes. Rev bras
Coloproct; 22 (1): 20-6, 2002.
10 Forones NM, Tanaka M, Machado D, Falcão JB &
Giovanoni M. Antígeno carcinoembrionário no diagnóstico
e acompanhamento do câncer colorretal. Arq
Gastroenterol; 34: 3-6, 1997.
11 Osanaga E, Larre Borges A, Sanguinetti J, Mancusso G,
Lopez A, Larreborges U. Étude comparative entre la
phosphatase alcaline et la gamma-glutamyl-transpeptidase dans
le diagnostic des metástases
hépatiques. J Chir (Paris); 122 (1): 17-20, 1985.
12 Herrera MA, Chu TM & Holyoke D.
Carcinoembryonic antigen (CEA) as a prognostic and monitoring test in
clinically complete resection of colorectal
carcinoma. Ann Surg; 183 (1): 5-9, 1976.
13 Corman ML _ Colon & Rectal Surgery. 3 ed.,
Philadelphia, Lippincott, 1992.
14 Abreu G, Dantas ANM, Jesus R, Lago PA. Análise do
valor prognóstico da dosagem sérica pré-operatória do
antígeno carcinoembrionário (CEA) em pacientes com
carcinoma colorretal. Rev bras Coloproct, 22(2): 82-7, 2002.
15 Wolmark N, Fisher B, Wieand S & Henry RS. The
prognostic significance of preoperative carcinoembryonic antigen
levels in colorectal cancer. Ann Surg; 199:375, 1984.
16 American Society of Clinical Oncology.
Recommended colorectal cancer surveillance guidelines. Disponível em:
< http://www.asco.org >. Acesso em: 12 nov.2002.
Endereço para correspondência:
Sandra Pedroso de Moraes
Rua Boaventura do Amaral, 684 / 131 - Centro
13.015-191 - Campinas (SP)
E-mail: spmoraes@nipnet.com.br
Trabalho realizado na Faculdade de Medicina do Centro de Ciências
da Vida da Pontifícia Universidade Católica de Campinas - Serviço de
Colo-Proctologia do Hospital e Maternidade Celso Pierro.


