ARTIGOS ORIGINAIS
AVALIAÇÃO IMUNOISTOQUÍMICA DA PROTEÍNA CICLOOXIGENASE-2 NAS NEOPLASIAS COLORRETAIS E SUA RELAÇÃO COM FATORES PATOLÓGICOS PROGNÓSTICOS
Immunohistochemical Evaluation of Cyclooxygenase-2 in Colorectal Neoplasias and Relationship with Pathological Factors in Prognosis
Brambilla, E1; Moreira, Luis Fernando2; Serafini, Eduardo Pretto3.
1 Professor da UEM Aparelho Digestivo da Universidade de Caxias do Sul; Membro Titular da Sociedade Brasileira de Coloproctologia; 2Professor do Curso de Pós-Graduação em Cirurgia da Universidade Federal do Rio Grande do Sul; 3Professor do departamento de Patologia da Universidade de Caxias do Sul.
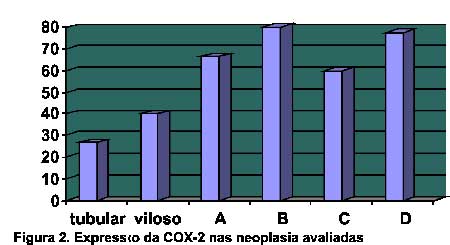
Resumo: Objetivos: Avaliar a prevalência da proteína ciclooxigenase-2 (COX-2) nas neoplasias colorretais e sua relação com os parâmetros patológicos prognósticos para o câncer colorretal. Métodos: 65 lesões neoplásicas colorretais foram avaliadas através de imunoistoquímica para a presença de COX-2, também foram analisados fatores patológicos prognósticos e estadiamento das lesões. Resultados: A COX-2 expressou-se positivamente em 27% dos adenomas tubulares, 40% dos adenomas vilosos e 70% nos carcinomas. Diferença estatisticamente significante foi obtida na expressão da COX-2 entre adenomas e carcinomas, porém não houve significância nas demais variáveis estudadas. Conclusão: A expressão da COX-2 parece variar progressivamente com a progressão da lesão neoplásica, mas não influencia os parâmetros patológicos de mau prognóstico.
Descritores: Ciclooxigenase-2, câncer colorretal, imunoistoquimica, carcinogenese.
Introdução
A neoplasia de cólon e reto constitui a
terceira causa de mortalidade por câncer no mundo e nos
Estados Unidos é responsável pelo aparecimento
de 130.000 novos casos por ano e por cerca de
56.000 mortes1. Devido a esta freqüência elevada,
métodos que possam trazer novas perspectivas nos campos
do diagnóstico precoce, estadiamento, tratamento
e profilaxia desta patologia tornam-se de grande interresse.
Estudos epidemiológicos têm demonstrado
uma incidência menor de adenomas e carcinomas em
indivíduos que usam cronicamente antiinflamatórios
não esteróides
(AINES)2,3,4. Também trabalhos com
indivíduos portadores de polipose adenomatosa
familiar, uma doença pré-maligna, mostram uma regressão
no número e tamanho dos pólipos quando submetidos
ao uso crônico de AINES5.
Os AINES possuem como mecanismo de
ação a inibição da enzima ciclooxigenase (COX). A
COX possui duas isoformas que são derivadas de genes
diferentes, mas possuem uma homologia de 60% em
sua estrutura. A COX-1 é expressa constitutivamente
nos tecidos, enquanto a COX-2 é usualmente ausente
ou expressa em quantidades muito
pequenas6,7. A COX-2 é induzida por estímulos pró-inflamatórios
como citocinas e fatores de crescimento, bem como se
apresenta elevada em uma grande variedade de
neoplasias como nas lesões
colorretais8. Em vários
experimentos que avaliam a deleção do gene da COX-2 ou a
inibição seletiva da proteína COX-2, observou-se redução
significativa no crescimento dos pólipos e no
desenvolvimento de tumores9,10,11.
Ainda persistem dúvidas sobre o
verdadeiro papel da COX-2 no aparecimento e progressão
dos tumores colorretais. Neste estudo avaliou-se a
expressão da COX-2 nos diferentes estágios da
neoplasia colorretal, relacionando-a também com fatores
prognósticos conhecidos como tipo de crescimento
tumoral, presença de padrão microacinar, caráter mucinoso
do tumor e presença de estroma fibrótico.
Metodologia
Este trabalho consiste em um estudo de prevalência onde os fatores em estudo são as
características patológicas do tumor primário e o
desfecho é a expressão imunoistoquímica da
proteína ciclooxigenase-2.
Foram avaliados 35 pacientes portadores de adenocarcinoma de cólon ou reto, e 30 pacientes
portadores de pólipos adenomatosos nos mesmos
segmentos ressecados cirúrgica ou endoscopicamente. As
lâminas para a análise da proteína COX-2 foram
preparadas a partir de blocos de parafina da peças
cirúrgicas ou ressecções endoscópicas.
Foram incluídos os pacientes com adenocarcinoma ou adenoma de cólon e reto e
foram excluídos da amostra os que preenchiam os critérios
a seguir: a) neoplasias que não fossem
diagnosticadas como adenomas ou adenocarcinoma; b)
outras neoplasias concomitantes ou tumores prévios;
c) neoplasia maligna sincrônica ou metacrônica do
intestino grosso; d) portadores de doença inflamatória
intestinal ou; e) polipose de qualquer tipo; f) história
familiar de neoplasia de cólon ou reto; g)
terapia neoadjuvante; ou ainda h) uso crônico de AINES.
As variáveis estudadas foram: idade,
gênero, localização, grau histológico, produção de muco,
caráter infiltrativo da lesão, aspecto do estroma,
padrão microacinar, presença de metástases linfáticas ou
a distância, estágio e expressão imunoistoquimica da
proteína COX-2; todas coletadas em revisão de
prontuários médicos e avaliação das lâminas existentes e
escolha dos blocos mais representativos de cada lesão
e avaliação histopatológica, respectivamente.
Os cortes dos blocos de parafina estocados das peças cirúrgicas foram submetidos à
avaliação imunoistoquímica utilizando-se o anticorpo
monoclonal anti-COX-2 (IgG, Dako Lab., New York, USA).
Para determinação da positividade destes anticorpos nos
tecidos, foi utilizado o método imunoistoquímico
ABC (avidin-biotin-peroxidase complex; kit LSAB
DAKO), conforme se segue.
Para aderência dos cortes dos blocos de
parafina às lâminas foi utilizado o organo selano.
Para desparafinização, as lâminas foram colocadas em
estufa a 37°C por 24 h e a 56°C por 3 h. Para reidratação
dos cortes as lâminas foram colocadas em etanol 100%,
etanol 95%, etanol 70%, água corrente e água destilada por
5 min cada. A fim de realizar a recuperação antigênica,
as lâminas foram colocadas em tampão citrato com pH 6,0
e levadas ao forno de banho-maria por 40 min a uma
temperatura de 95°C. Para bloquear a peroxidase
endógena as laminas foram tratadas com peróxido de
hidrogênio 5% em metanol por 20 min em câmara escura, com
uma repetição. Os cortes foram circulados com caneta
Dako Pen (DAKO lab. Inc., New York, NY, USA) e
incubados em câmara úmida e escura por 16 h com o
anticorpo primário anti-COX-2 (IBL, JAPAN) diluído em 1:50,
em SAB (albumina bovina 1%). A seguir, as lâminas
foram encubadas com o primeiro anticorpo do kit LSAB
(DAKO) em câmara úmida durante 30 min. Estes passos
foram intercalados por duas ou três lavagens das lâminas
em SST por 5 min, que logo foram encubadas com a streptavidina do kit LSAB em câmara úmida por 30
min, após terem sido novamente lavadas duas vezes em
SST por 5 min. O cromógeno tetrahidrocloreto
de diaminobenzedina (DAB) foi pingado nas lâminas
para colorir a reação por 5 min e após, a reação foi
bloqueada em água destilada. Em seguida as lâminas
foram encubadas por 30 seg em hematoxilina de Harris e
lavadas em água corrente. Por fim, foram mergulhadas
em água amoniacal (20% de hidróxido de amônia em
água destilada) e lavadas em água corrente, álcool e xilol
para posterior montagem.
As lâminas e os prontuários foram
avaliados para confirmação do laudo original do estágio e
diagnóstico realizado. As lesões adenomatosas foram
divididas em tubulares e vilosas. No grupo dos
carcinomas o sistema de estadiamento utilizado foi de Dukes
modificado por Astler-Coller, e este acrescido covencionalmente do estágio D pra traduzir a
presença de metástases a distância.
A partir do laudo anatomopatológico, os
casos de adenocarcinoma foram divididos em bem
diferenciados, moderadamente e pouco diferenciados; e
os adenomas classificados em displasias de baixo grau
e alto grau. Também avaliou-se a presença de
componente mucinoso, estroma fibrótico, padrão
microacinar e invasão infiltrativa da margem.
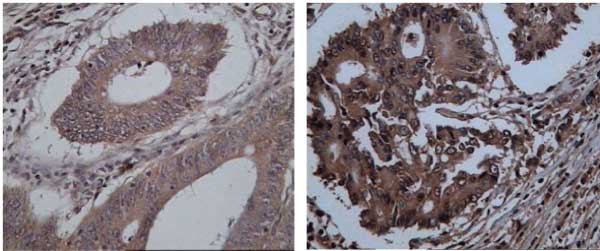
A reação imunoistoquímica para COX-2
apresentou imagem granular no citoplasma de
coloração acastanhada produzida pelo DAB, com
intensidade variável. Foram considerados positivos os casos
em que houve coloração de 10% das células contadas
de maneira manual em campo microscópico de 400X
na área total da lâmina (Figura 1). Como controle
positivo foi utilizado um caso de adenocarcinoma de reto
do arquivo do serviço de patologia. Os controles
negativos foram obtidos a partir de biópsias de mucosa
normal presente no arquivo do laboratório de
patologia. Para fins diagnóstico, as lâminas foram avaliadas
por patologista com experiência em diagnóstico
por imunoistoquímica.
 |
Figura 1 (A e B) - Fotomicrografia de caso representativo de adenoma tubular COX-2 positivo (IHC 400X) _ Fotomicrografia de
caso representativo de adenocarcinoma COX-2 positivo (IHC-400X). |
 |
 |
 |
 |
 |
Abstract: Objectives: To evaluate the prevalence of cyclooxygenase-2 (COX-2) in colorectal neoplasia and to establish the relationship with pathological factors in the prognosis of colorectal cancer. Methods: 65 colorectal neoplastic lesions were investigated by immunohistochemistry for the expression of COX-2, along with the pathological factors in prognosis and staging of lesions. Results: COX-2 was positively expressed in 27% of tubular adenomas, 40% of villous adenomas, and 70% of carcinomas. A statistically significant difference was observed among COX-2 expression in adenomas and carcinomas, but such significance was not seen among the other variables studied. Conclusion: COX-2 expression seems to correlate positively with the progression of neoplasias, yet with no influence on the pathological patterns of poor prognosis.
Key words: Cyclooxygenase-2, colorectal cancer, immunohistochemistry, carcinogenesis.
Referências
1. LANDIS SH, MURRAY T, BOLDEN S, WINGO PA.
Cancer Statistics, 1999. CA Cancer J Clin 1999; 49: 8-31.
2. GIOVANNUCCI E, RIMM EB, STAMPFER MJ, COLDITZ GA, ASCHERIO A, WILLETT WC. Aspirin
use and the risk for colorectal cancer and adenomas in male
health professionals. Ann Intern Med 1994; 121: 241-6.
3. SMALLEY V, RAY WA, DAUGHERTY J, GRIFFIN
MR. Use of nonsteroidal anti-inflammatory drugs and incidence
of colorectal cancer: A population-based study. Arch Intern
Med 1999; 159:161-6.
4. STURMER T, GLYNN RJ, LEE I, MANSON JE,
BURING JE, HENNEKENS CH. Aspirin use and colorectal
cancer: Post-trial follow-up data from the physician's health
study. Ann Intern Med 1998; 128: 713-20.
5. GIARDELLO FM, HAMILTON SR, KRUSH AJ, PIANTADOSI S, HYLIND LM, CELANO P, et al.
Treatment of colonic and rectal adenomas with sulindac in
familial adenomatous polyposis. N Engl J Med 1993; 328: 1313-6.
6. VANE JR, BOTTING RM. Mechanism of action
of nonsteroidal anti-inflamatory drugs. Am J Med 1998;
104: 2s-8s.
7. SMITH WL. Prostanoid biosynthesis and mechanisms
of action. Am J Physiol 1992; 263: F181-91
8. RIGAS B, GOLDMAN IS, LEVINE L. Altered
eicosanoid level in human colon cancer. J Lab Clin Med 1993; 122:
518-23.
9. WINDE G, SCHIMID KW, SCHEGEL W, FISCHER
R, OSSWALD H, BÜNTE H. Complete reversion and
prevention of rectal adenomas in colectomized patients with
familial adenomatous polyposis by rectal low-dose sulindac
maintence treatment. Dis Colon Rectum 1995; 38: 813-30.
10. PASRICHA PJ, BEDI A, O`CONNOR K, RASHID
A, AKHTAR AJ, ZAHURAK ML. et al. The effects of
sulindac on colorectal proliferation and apoptosis in familial
polyposis. Gastroenterol 1995; 109: 995-8.
11. OSHIMA M, DINCHUK JE, KARGMAN SL,
OSHIMA H, HANCOCK B, KWONG E, et al. Supression of
intestinal polyposis in APCÄ716 knockout mice by inhibition
of cyclooxygenase 2 (COX-2). Cell 1996; 87: 803-9
12. FERRANDINA G, LAURIOLA L, ZANNONI F, FAGOTTI
A, FANFANI F, LEGGE F, et al. Increased cyclooxigenase-2
(cox-2) expression is associated with chemotherapy resistance and
outcome in ovarian cancer patients. Ann Oncol 2002; 13: 1205-11.
13. SING-RANGER G, MOKBEL K. The role of
cyclooxigenase-2 (cox-2) in brest cancer, and implications of cox-2
inhibition. EJSO 2002; 28: 29-737.
14. SHEEHAN KM, SHEEHAN K, O'DONOGHUE DP, MACSWEENEY F, CONROY RM, FITZGERALD DJ,
et al. The relationship between cyclooxygenase-2 expression
and colorectal cancer. JAMA 1999; 282: 1254-7.
15. YAMAUCHI T, WATANABE M, KUBOTA T, HASEGAWA H, ISHII Y, ENDO T, et al.
Cyclooxigenase-2 expression as a new marker for patients with colorectal
cancer. Dis Colon Rectum 2002; 45: 98-113.
16. MASUNAGA R, KOHNO H, DHAR DK, OHNO S, SHIBAKITA M, KINUGASA S, et al.
Cyclooxigenase-2 expression correlates with tumor neovascularization
and prognosis in human colorectal carcinoma patients. Clin
Cancer Res 2000; 6: 4064-68.
17. ZHANG H, SUN XF. Overexpression of
cyclooxigenase-2 correlates with advanced stages of colorectal cancer. Am
J Gastroenterol 2002; 97: 1037-41.
18. TOMOZAWA S, TSUNO NH, SUNAMI E, HATANO
K, KITAYAMA J, OSADA T, et al. Cyclooxigenase-2
overexpression correlates with tumor recurrence, especially
haematogenous metastasis, of colorectal cancer. British J Cancer 2000; 83: 324-8.
19. HULL MA, FENWICK SW, CHAPPLE KS, SCOTT
N, TOOGOOD GJ, LODGE JP. Cyclooxigenase-2
expression in colorectal cancer liver metastases. Clinical
Experimental Metastasis. 2000; 18: 21-7.
20. PETERSEN S, HAROSKE G, HELLMICH G, LUDWIG
K, PETERSEN C, EICHELER W. Cox-2 expression in
rectal carcinoma: Immunohistochemical pattern and clinical
outcome. Anticarcer Reserch 2002; 22: 1225-30.
21. FUJITA M, FUKUI H, KUSAKA T, UEDA Y,
FUJIMORI T. Immunohistochemical expression of cyclooxygenase
(cox)-2 in colorectal adenomas. J gastroenterol 2000; 35: 488-90.
22. KHAN KNM, MASFERRER JL, WOERNER BM, SOSLOW R, KOKI AT. Enhanced cyclooxigenase-2
expression in sporadic and familial adenomatous polyposis of the
human colon. Scand J Gastroenterl 2001; 36: 865-9.
23. JURACH MT. Expressão do P53 e relação
clínico-patológica no adenocarcinoma de reto: resultados preliminares.
Dissertação de mestrado. Universidade Federal do Rio Grande do
Sul. Programa de pós-graduação em medicida: cirurgia. 2003.
24. HASEGAWA K, ICHIKAWA W, FUJITA T. Expression
of cyclooxigenase-2 (cox-2) mRNA in human
colorectal adenomas. Euro J Cancer 2001; 37: 1469-74.
25. HULL MA, FENWICK SW, CHAPPLE KS, SCOTT
N, TOOGOOD GJ, LODGE JP. Cyclooxigenase-2
expression in colorectal cancer liver metastases. Clinical
Experimental Metastasis. 2000; 18: 21-7.
26. DIMBERG J, SAMUELSSON A, HUGANDER A, SÖDERKVIST. Differential expression of cyclooxigenase
2 in human colorectal cancer. Gut 1999; 45: 730-2.
27. HULL M, LANGMAN M. Differential expression
of cyclooxygenase 2 in human colorectal cancer. Gut 2000; 47: 154-8.
28. SINICROPE FA, LEMOINE M, XI L, LYNCH PM,
CLEARY KR, SHEN Y, et all. Reduced expression of cyclooxigenase
2 protein in hereditary nonpolyposis colorectal cancers
relative to sporadic cancers. Gastroenterol 1999; 117: 350-8.
29. KARNES WE. Implications of low cox-2 expression
in colorectal neoplasms with defective DNA mismatch repair.
J Cell Biochem Suppl 2000; 34: 23-7.
30. KARNES WE, SHATTUCK-BRANDT R, BURGART
LJ, DUBOIS RN, TESTER DJ, CUNNINGHAM JM, et all. Reduced cox-2 protein in colorectal cancer with
defective mismatch repair. Cancer Res 1998; 58: 5473-7.
31. SHAO J, SHENG H, ARAMANDIA R, PEREIRA
MA, LUBET RA, HAWK E, ET AL.. Coordinate regulation
of cyclooxygenase-2 and TGF-â1 in replication
error-positive colon cancer and azoxymethane-induced rat colonic
tumors. Carcinogenesis 1999; 20: 185-91.
32. YANG VW, SHIELDS JM, HAMILTON SR,
SPANNHAKE EW, HUBBARD WC, HYLIND LM, et all. Size-dependent
increase in prostanoid levels in adenomas of patients with
familial adenomatous polyposis. Cancer Res 1998; 58: 1750-3.
33. DOBBIE Z, MULLER PY, HEINIMANN K,
ALBRECHT C, D`ORAZIO D, et all. Expression of cox-2 and wnt
pathway genes in adenomas of familial polyposis patients treated
with meloxicam. Anticancer Res 2002; 22: 2215-20.
34. HSI LC, ANGERMAN-STEWART J, ELING TE. Introduction of full-length APC modulates
cyclooxygenase-2 expression in HT-29 human colorectal carcinoma cells at
the translational level. Carcinogenesis 1999; 20: 2045-9.
Endereço para correspondência:
Rua General Arcy da Rocha Nóbrega, 401/705
Madureira - Caxias do Sul/RS
95040-000
Fone/Fax: (54) 3222 9874
E-mail: brambilla.procto@terra.com.br
Recebido em 13/06/2007
Aceito para publicação em 20/07/2007
Trabalho realizado no Hospital Geral de Caxias do Sul. Universidade de Caxias do Sul.