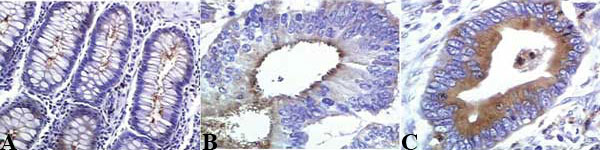
A: Polarização celular do CEA no colonócito normal. (Imunohistoquímica para CEA, 100x).
B: Carcinoma bem polarizado.
C: Carcinoma moderadamente polarizado (Imunohistoquímica para CEA, 400x).
ARTIGOS ORIGINAIS
PROPOSTA PARA ESTADIAMENTO DO CÂNCER COLORRETAL BASEADA EM CRITÉRIOS MORFOFUNCIONAIS. CORRELAÇÃO COM NÍVEIS SÉRICOS DO ANTÍGENO CARCINOEMBRIONÁRIO
Proposal for Colorectal Cancer Stages Based on Morphofunctional Criteria. Correlation with Carcinoembryonic Antigen Levels
Denise GonÇalves Priolli1; Izilda Aparecida Cardinalli2; Helenice Piovesan3; Nelson Fontana Margarido4, Carlos Augusto Real Martinez5
1. Professor Adjunto Doutor Colaborador do Programa de Pós-graduação em Ciências da Saúde da Universidade São Francisco, Bragança Paulista, São Paulo; 2. Professor Assistente Doutor Colaborador do Programa de Pós-graduação em Ciências da Saúde da Universidade São Francisco, Bragança Paulista, São Paulo. 3. Professor Assistente da Disciplina de Patologia Universidade São Francisco, Bragança Paulista, São Paulo, Brasil. 4. Professor Livre-Docente do Departamento de Cirurgia da Faculdade de Medicina da Universidade de São Paulo, São Paulo, Brasil. 5. Professor Adjunto Doutor do Programa de Pós-graduação em Ciências da Saúde da Universidade São Francisco, Bragança Paulista, São Paulo.
RESUMO: A análise de características morfofuncionais pode ser útil na predição evolutiva do câncer colorretal, especialmente se relacionadas aos níveis séricos de antígeno carcinoembrionário. A pesquisa de instabilidades de cromossomos e genes e alterações da expressão tecidual de proteínas por eles codificadas, tornam atraente a possibilidade do emprego de fatores funcionais como variáveis potencialmente válidas na compreensão do prognóstico do carcinoma colorretal.1 Objetivo: Propor estadiamento baseado nas características morfológicas e funcionais do carcinoma colorretal, valorizando o poder prognóstico do antígeno carcinoembrionário. Método: Acompanhou-se 35 pacientes em estágios diferentes da evolução do adenocarcinoma colorretal no período de 2001 a 2007. A medida sérica do antígeno carcinoembrionário foi executada pela técnica de quimioluminescência. Realizou-se estudo anatomopatológico para determinação do grau histológico e estádio TNM, e análise imunohistoquímica para determinação da polarização tecidual do antígeno carcinoembrionário. A classificação morfofuncional foi determinada pela combinação entre grau histológico e polarização do antígeno. O estadiamento morfofuncional baseou-se na associação entre classificação morfofuncional e estadiamento TNM, por pontuação atribuída a cada uma das classificações. As variáveis estudadas foram: CEA sérico, classificação morfofuncional, estadiamento TNM e morfofuncional. Os resultados foram analisados por análise variância, teste de correlação e análise de sobrevivência (Kaplan-Meier e Modelo de Regressão de Cox), adotando-se p>0,05% para rejeição da hipótese de nulidade. Resultados: A curva de sobrevida no estadiamento morfofuncional apresentou resultados semelhantes aos encontrados no estadiamento TNM. Houve relação entre a nova proposta de estadiamento e o tempo de sobrevida do paciente. Observou-se relação entre o tempo de sobrevida, a classificação morfofuncional e o nível sérico de antígeno carcinoembrionário. Conclusão: O estadiamento morfofuncional é válido para a avaliação prognóstica dos pacientes com adenocarcinoma colorretal, e relaciona-se com os níveis séricos do CEA.
Descritores: Antígeno carcinoembrionário, Imunohistoquímica, Análise de Sobrevida, Estadiamento de neoplasias, Prognóstico, Neoplasia colorretal.
INTRODUÇÃO
O câncer colorretal (CCR) nos Estados Unidos,atualmente, representa a segunda causa
de morte por neoplasia entre os homens e a terceira
entre as mulheres.2 Os índices de mortalidade vêm se
alterando lentamente, não obstante os recentes
avanços obtidos no diagnóstico precoce e
tratamento.3,4 No Brasil, a evolução do CCR tem apresentado
comportamento semelhante sendo, no momento, a quinta
causa mais comum de morte relacionada ao câncer.
À semelhança de outros países, sua incidência vem
aumentando em comparação a outros tipos de
tumores que acometem o aparelho
digestório.5
A variabilidade dos comportamentos clínico
e biológico do CCR tem suscitado grande interesse
pelo estudo de fatores que possam estar associados à
progressão da neoplasia e, conseqüentemente, ao
prognóstico da doença.6,7 Estudos têm sido
publicados correlacionando variáveis clínicas e
histopatológicas ao prognóstico do CCR, mas seus resultados são
intrigantes e muitas vezes
conflituosos.8,9 O diagnóstico
precoce,10 a idade,11 localização da
neoplasia,12 graduação
histológica,13 grau de penetração na parede intestinal,14comprometimento
linfonodal,15 produção de muco pela
neoplasia,16 antígeno carcinoembrionário
(CEA),17 invasão venosa e
neural18 são as variáveis mais freqüentemente
estudadas, como fatores relacionados ao prognóstico
da enfermidade. Estudos foram realizados com o
intuito de discriminar o poder prognóstico independente
das principais variáveis relacionadas ao
CCR.19,20 O consenso dessas publicações revela que os fatores
que apresentam associação com a evolução dos
doentes são: profundidade de infiltração do tumor na
parede intestinal, o comprometimento linfonodal, a
presença de metástases e a graduação histológica
da neoplasia.18,19 Entretanto, as tentativas de
avaliação prognóstica baseadas puramente em
aspectos morfológicos, apresentam a grave limitação de
restringirem-se à observação de um registro
microscópico momentâneo da morfologia tumoral, não
fornecendo informações sobre o real comportamento
biológico do tumor, o qual se encontra relacionado a
mecanismos intrínsecos de funcionamento das
células componentes daquele
tecido.19 Recentemente, com a melhor compreensão das alterações genéticas
envolvidas na carcinogênese colorretal, a pesquisa de
instabilidades de cromossomos e genes, bem como as alterações da expressão tecidual de proteínas por
eles codificadas vêm tornando atraente a possibilidade
do emprego de fatores funcionais como variáveis
potencialmente válidas para a melhor compreensão do
prognóstico do CCR.21 Com o advento dos métodos
de análise indireta da expressão de genes, pela
detecção tecidual das proteínas por eles codificadas com
técnicas imunohistoquímicas, nova dimensão no estudo
da carcinogênese colorretal foi conquistada. A
possibilidade da avaliação funcional de antígenos
relacionados ao desenvolvimento, crescimento e
disseminação do tumor permite verificar sua importância como
fator relacionado ao prognóstico da
enfermidade.20
O CEA, de todos os marcadores tumorais, é
o mais freqüentemente utilizado no seguimento de
doentes com CCR. Desde a sua descrição por Gold
e Freedman, em 1965,22 ainda não se encontra bem
esclarecido o mecanismo pelo qual o
antígeno carcinoembrionário produzido pelas células normais
ou neoplásicas da mucosa do trato disgestório atinge a
circulação sangüínea. Da mesma forma, existem
dúvidas quanto à importância dos níveis elevados do CEA
no pré-operatório como variável independente
relacionada ao prognóstico da doença. Estudos vêm avaliando
o poder prognóstico da quantificação sérica do
CEA, correlacionando-o a variáveis
morfológicas estabelecidas, representadas pelas diferentes
formas de estadiamento, demonstrando associação entre
níveis elevados do antígeno e prognóstico
desfavorável, entretanto, os resultados são controversos e ainda
despertam polêmica.23,24,25
Níveis circulantes crescentes de CEA, após
a extirpação completa da lesão, podem sugerir
recidiva da neoplasia.26 Entretanto, existe percentual de
CCR escassamente produtores do CEA, que cursam com níveis séricos normais, nos quais a
mensuração sangüínea do antígeno encontra-se pouco
relacionada a possibilidade de detecção de doença avançada
ou recidiva.27 Neoplasias com pior grau histológico
podem se tornar escassamente produtoras de CEA, em virtude do seu distanciamento da célula normal
da mucosa cólica.28 Dessa forma, a relação entre
níveis séricos do CEA e estádio do CCR permanece
incerta ao se considerarem tumores com
características histológicas e funcionais distintas. Atualmente, os
estudos que correlacionam o CEA ao prognóstico do
CCR são dirigidos não apenas a mensuração dos
níveis séricos do CEA, mas também a presença do
antígeno no tecido tumoral, onde assumem aspectos
importantes como capacidade de produção e excreção
pela célula neoplásica.27
O estadiamento TNM, apesar de ainda ser o melhor e mais utilizado indicador de prognóstico,
apresenta-se falho na estimativa da evolução de
muitos pacientes, especialmente nos estádios clínicos II e
III, dificultando a indicação terapêutica de forma
adequada e consensual.29,30 Dessa forma, é necessária a
incorporação de novos fatores que considerem de
forma conjunta aspectos histopatológicos e funcionais.
Proposta de estadiamento que considere características morfológicas e funcionais associadas,
baseada em critérios relacionados ao prognóstico do
CCR, tais como grau histológico da neoplasia,
imunoexpressão e excreção tecidual do CEA, permitiria categorizar
estádios baseados não somente nos
aspectos histopatológicos, mas também em aspectos
funcionais. Esta estratificação, considerando
aspectos morfofuncionais, responderia a questão dos
diferentes comportamentos de tumores supostamente
semelhantes de forma mais precisa.
A partir da combinação de
variáveis morfológicas sabidamente reconhecidas como
relacionadas ao prognóstico (estadiamento TNM) e
variáveis relacionadas à dinâmica funcional do CEA
(classificação morfofuncional) seria possível estabelecer a
correta estratificação das neoplasias em grupos de
comportamentos biológicos semelhantes, permitindo,
dessa maneira, maior fidedignidade nas projeções
relacionadas ao prognóstico da doença.
O objetivo do presente estudo foi estabelecer proposta de estadiamento do CCR baseado em
suas características morfológicas e funcionais,
valorizando o poder prognóstico das dosagens séricas do CEA.
MÉTODO
A realização desse estudo obedeceu todas
as etapas previstas pelo Comitê de Ética em Pesquisa
da Universidade São Francisco, e as exigências do
Conselho de Ética em Pesquisa da Comissão Nacional
de Ética em Pesquisa (CONEP) do Ministério da
Saúde. (Resolução CNS196/96).
Foram estudados 35 doentes com CCR, classificados em estágios diferentes da evolução da
doença (TNM), acompanhados após o diagnóstico
da neoplasia no período 2001 a 2007. Não se fez
qualquer tipo de seleção quanto à idade, sexo e raça.
Foram excluídos os pacientes com CCR com idade menor
que 18 anos, pacientes cujo número de linfonodos
ressecados fosse menor que 12, ou aqueles que não
tiveram como causa mortis o CCR. Doentes que
apresentaram doença metastática irressecável no fígado
foram submetidos à biópsia local para posterior
confirmação histopatológica.
A mensuração do nível de CEA sérico foi
realizada pela técnica de quimioluminescência. As
amostras sangüíneas foram colhidas por punção venosa
imediatamente antes da operação e encaminhadas
prontamente ao laboratório de análises.
O estudo anatomopatológico convencional
(HE) obedeceu a protocolo previamente elaborado, de
maneira que todos os doentes tiveram os mesmos parâmetros estudados. O CCR foi avaliado quanto
grau histológico sendo classificados em bem
diferenciados, moderadamente diferenciados ou indiferenciados,
segundo a extensão de sua aparência glandular. Os
tumores produtores de muco foram considerados como indiferenciados, de acordo com a orientação da
OMS. Todos os casos estudados foram classificados
segundo estadiamento TNM.
A técnica imunohistoquímica foi realizada
conforme metodologia anteriormente descrita,
empregando-se a técnica de
estreptavidina-biotina-peroxidase (ABC) utilizando anticorpo monoclonal anti-CEA
(Dako Cytomation. Monoclonal Rabit
Carcinoembrionic Antigen. Clone II-7. Código
A-115).31
Considerou-se positiva a presença do CEA
no tecido quando a imunocoloração identificou
granulação homogênea acastanhada tanto no tecido normal
quanto neoplásico. A análise microscópica das lâminas
foi realizada com o auxílio de um microscópio óptico
comum, com ajuda de lente objetiva de 100x e com magnificação final de 400x. A leitura de todas as
lâminas foi sempre realizada por dois patologistas, de
forma consensual, experimentados na
interpretação imunohistoquímica.
A polarização do CEA foi avaliada,
comparando-se o distanciamento da capacidade de excreção
do colonócito normal, ou seja, a alteração da dinâmica
funcional avaliada pela perda da direção polarizada
do antígeno no tecido neoplásico.
No tecido normal o antígeno foi
identificado como uma linha de imunocoloração restrita a
membrana ápico-luminal da célula cólica, demonstrando a
dinâmica de migração do CEA celular com
orientação polarizada, atingindo a região apical da célula (figura
1, foto A). No tecido neoplásico, considerou-se como
bem polarizados os carcinomas com manutenção parcial
da capacidade de polarização do CEA com acúmulo
dos grânulos imunocorados na região
ápico-citoplasmática (figura 1, foto B); como moderadamente
polarizados, os CCR com distribuição dos grânulos de
CEA difusamente imunocorados no citoplasma celular
(figura 1, foto C); e como pouco polarizados, aqueles
que apresentavam distribuição celular cordonal, pela
impossibilidade de se diferenciar o pólo apical do pólo
basal celular e neoplasias que, à histologia convencional,
representam o padrão mucinoso do CCR.
 |
Figura 1 - Polarização celular do CEA tecidual do CEA. A: Polarização celular do CEA no colonócito normal. (Imunohistoquímica para CEA, 100x). B: Carcinoma bem polarizado. C: Carcinoma moderadamente polarizado (Imunohistoquímica para CEA, 400x). |
Os CCR foram agrupados em três classes morfofuncionais de acordo com a funcionalidade
e morfologia, baseados na capacidade celular de
polarização do antígeno, avaliada pela
técnica imunohistoquímica e, o grau histológico, avaliado
pela técnica de HE. Carcinomas bem diferenciados e
bem polarizados e, moderadamente diferenciados e
bem polarizados constituem a classe morfofuncional 1,
enquanto carcinomas moderadamente diferenciados e moderadamente polarizados e, neoplasias bem
diferenciadas e moderadamente polarizadas compõem a
classe morfofuncional 2; a classe 3 foi constituída por
carcinomas moderadamente diferenciados ou mucoprodutores pouco polarizados e,
carcinomas indiferenciados pouco polarizados (Quadro 1).
 |
O estadiamento morfofuncional foi proposto a partir da associação da classificação morfofuncional
e o estadiamento TNM, por meio de pontuação
atribuída a cada uma das classificações. A somatória igual a
1 (classe morfofuncional 1 (1 ponto) + Estádio TNM
0 (0 ponto), representa o estádio morfofuncional I,
enquanto no outro extremo, com somatória igual a 7
(classe morfofuncional 3 (3 pontos) + TNM IV (4
pontos), compõe o estádio IV do estadiamento
morfofuncional (Quadro 2).
 |
Na análise dos resultados obtidos
adotou-se valor de p menor que 5% para a rejeição da
hipótese de nulidade. As variáveis analisadas foram CEA
sérico, classe morfofuncional (baseada na polarização
celular do CEA e grau histológico da neoplasia),
estadiamento TNM, estadiamento morfofuncional e curva de
sobrevivência. Os resultados encontrados foram
analisados utilizando análise descritiva, análise de variância,
regressão linear, curva de sobrevivência
de Kaplan-Meyer, Log-Ranks, Modelo de Cox.
RESULTADOS
Dos 35 casos acompanhados, 24 (68,6%) se mantêm vivos, houve 9 (25,7%) óbitos e 2 (5,7%)
casos se perderam no acompanhamento do
2o ano. Dezessete casos (48,6%) foram classificados
como pertencentes à classe morfofuncional 1, 15
(42,9%), à classe 2 e três (8,6%) à classe
3 (Tabela 1). Quanto ao TNM, 65,7% (23) dos casos pertenciam ao
estádio 2; 8 casos (22,9%) ao estádio 3 e 4 casos
(11,4%) ao estádio 4 (Tabela 2).
 |
 |
A taxa de sobrevivência baseada no estadiamentos TNM e morfofuncional demonstrou
diferença quanto aos estádios avaliados,
respectivamente, p=0,001 e p=0,002 (figura 2). A regressão de
Cox demonstrou significância entre o tempo de
sobrevida, a classificação morfofuncional e o nível sérico de
CEA (p=0,002)
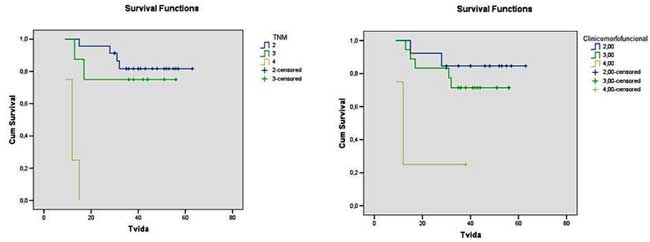 |
Figura 2 - Curvas de sobrevivência de acordo com os estadiamentos TNM e morfofuncional |
DISCUSSÃO
O CEA é um dos marcadores tumorais
melhor estudados em câncer, sendo rotineiramente
utilizado como marcador sérico do carcinoma gastrintestinal,
em especial do CCR.23,32 Devido à baixa
especificidade, não é utilizado como teste diagnóstico, sendo
atualmente aplicado na prática clínica no seguimento dos
enfermos submetidos ao tratamento cirúrgico do
CCR.33 Níveis crescentes do marcador, após a extirpação
da lesão, podem sugerir recidiva da neoplasia.
Contudo, existe um percentual de tumores colorretais que
produzem quantidades pouco expressivas do CEA,
determinando níveis séricos baixos, nos quais é pequena
a possibilidade de detecção de doença avançada ou
recidiva com esse recurso.23,26
Há contradições na correlação entre o
nível sérico, expressão do CEA no tumor revelado pela
análise imunohistoquímica com anticorpos
monoclonais anti-CEA e prognóstico das lesões
neoplásicas colorretais.27,34
A face celular voltada para a luz intestinal
apresenta especializações ou microvilosidades
relacionadas aos fenômenos de absorção e excreção, próprios
da mucosa cólica. As células da mucosa normal do
colo sintetizam constantemente o antígeno que migra
pelo citoplasma e associa-se à membrana celular,
sendo então eliminado no lume
intestinal.35 Obedecendo a características de epitélio colunar especializado,
proteínas produzidas nas células mucosas do colo têm
orientação de direção polarizada no sentido
ápico-lateral. Como qualquer outra proteína, o sentido vetorial do
CEA no interior da célula também respeita esta
orientação. Essa característica das células que compõem a
mucosa do intestino grosso é mantida pela constante
movimentação compartimentada do CEA produzido nas
porções basais das células, que migra progressivamente para
o pólo apical para, a partir daí, ser eliminado para o
lume intestinal.36
No epitélio cólico normal observa-se
acúmulo progressivo do CEA no interior do citoplasma de
células com menor grau de diferenciação, sugerindo
que a incapacidade de polarização do antígeno possa
estar relacionada ao menor grau de diferenciação e
especialização celular.34,37
As células da mucosa cólica migram do interior das criptas para o ápice
das vilosidades. À medida que vão se especializando,
tornam-se mais diferenciadas quando comparadas
às células localizadas no interior das criptas, na zona
de epitélio proliferativo.38 Estudos demonstraram que
o padrão de distribuição tecidual do CEA e os
níveis séricos nos doentes com CCR podem estar
relacionados com o grau de diferenciação celular do
tumor.27,39,40 A relação existente entre
especialização celular, intensidade e padrão de expressão
tecidual vêm fazendo com que o CEA seja utilizado
como marcador importante nos estudos que avaliam a
diferenciação
celular.27,37,38,41 Outros autores,
entretanto, contradizem esta afirmativa.42,43
Tumores bem diferenciados e com padrão
de distribuição do tipo apical exibem níveis baixos do
CEA sérico, enquanto portadores de tumores
moderadamente diferenciados ou indiferenciados com padrão de
distribuição citoplasmático apresentam níveis séricos
elevados.39 Tumores bem diferenciados com
intensidade de expressão moderada a intensa, mas com padrão
de distribuição do tipo apical, podem cursar com
níveis baixos do CEA sérico, pois embora o antígeno
esteja presente no tecido, a maior parte dele é eliminada
para o lume intestinal.38
Demonstrou-se, em estudo in vitro, que a
matriz dos adenocarcinomas colorretais é originária
de células LISP-I, e que suas subpopulações,
LISP-A10 e LISP-E11 possuem características diferentes,
epitelial e fibroblástica, respectivamente. As células
LISP-A10 são produtoras de moléculas de adesividade
intercelular, como o CEA e a desmogleina, enquanto tumores
originados na população celular LISP-E11 produzirão
de maneira incipiente o CEA, aproximando-se do
padrão indiferenciado do CCR.26 Esses aspectos indicam
que não apenas a característica morfológica celular,
como a diferenciação celular, são importantes na
determinação dos níveis séricos do CEA, mas também a
capacidade das células neoplásicas de produzirem o
antígeno. Desta forma, uma classificação que considera
fatores morfológicos e funcionais poderia orientar o
verdadeiro significado prognóstico dos níveis circulantes
do CEA.
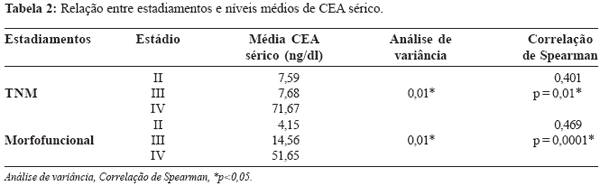
No presente estudo, os valores séricos do
CEA encontraram-se significantemente mais elevados
nas classes morfofuncionais mais avançadas (tabela
1). Desse modo fica reforçada a idéia que o
distanciamento da célula neoplásica do colonócito normal, do ponto
de vista morfofuncional, propicia o aporte de maiores
quantidades do CEA à corrente sanguínea, sugerindo
que diferentes expressões fenotípicas encontram-se
relacionadas aos níveis circulantes do marcador.
Apesar das controvérsias em relação à
validade das dosagens pré-operatórias do CEA, estudos
destacam seu valor e mostram associação entre nível
pré-operatório elevado do antígeno e prognóstico
desfavorável.24,27 Contradizem estes achados pesquisas
mostrando que 14% a 56% dos casos de CCR podem cursar com nível sérico de CEA
normal.23,44 A correlação dos níveis séricos do CEA pré-operatórios com o
estádio do carcinoma colorretal permanece polêmica.
Sugeriu-se a relação do CEA como parâmetro
prognóstico independente do
estádio,11 em contraposição
àqueles que mostraram a relação dos níveis séricos do
CEA em estádios mais avançados da doença
neoplásica colorretal.45,46
No presente corte, o nível sérico do CEA
variou de 0,1ng/dl em doente em estádio inicial a
106,0ng/dl em enfermo portador de metástase hepática.
Provavelmente tal associação é dependente do estádio
da neoplasia, uma vez que o nível do CEA sérico é
também determinado pelas dimensões do tumor primário
e lesões metastáticas que representam, na realidade,
a massa produtora do antígeno. Além disso, nas
neoplasias em estádio avançado, a infiltração a planos
profundos facilita o acesso do antígeno à circulação
angiolinfática e sua distribuição sistêmica, elevando seus
níveis séricos.30,44,47 Os resultados obtidos no presente
estudo, corroboraram essas afirmativas quando
verificou-se correlação entre estadiamento TNM
e morfofuncional e o nível sérico do antígeno, que
encontrou-se elevado nos estádios mais avançados
da neoplasia (tabela 2).
Os sistemas de estadiamento do CCR baseiam-se em informações referentes à extensão da
doença, sendo importantes no planejamento terapêutico,
na avaliação dos resultados obtidos com os
tratamentos propostos e no prognóstico. Muitas foram as
tentativas em sistematizar o CCR, cabendo a Dukes a mais
simples, que combina profundidade de invasão na
parede retal e metástase.13 Em 1945, a classificação de
Dukes foi estendida para o colo e quase 10 anos após,
Astler e Coller propuseram nova
modificação.14 Em busca
de maior acurácia quanto aos resultados obtidos com
as estratificações propostas, em 1966 foi publicado o
primeiro estadiamento TNM (Tumor, Linfonodo, Metástase) para o
CCR.48 O estadiamento TNM é baseado no nível de penetração da parede
intestinal (T), no número e localização de linfonodos
comprometidos (N), e na presença ou não de metástases à
distância (M).
Apesar de ser o estadiamento mais utilizado, o TNM tem acurácia aproximada de 65%, falhando
ao estimar a evolução de muitos
pacientes.28 A falha ocorre especialmente nos estádios clínicos II e III, não
permitindo consenso em relação a indicação de
quimioterapia adjuvante.29 Há necessidade de refinamento
do estadiamento anatomopatológico por meio da
associação de fatores funcionais, com estratificação em
grupos que permitam inferências sobre o prognóstico
com melhores índices de acerto. O consenso do
Colorectal Working Group, recomenda que o nível sérico do
CEA pré-operatório deva ser considerado como fator
prognóstico no estadiamento TNM.
No presente estudo, quando se incorporou os aspectos funcionais ao estadiamento TNM,
pôde-se demonstrar relação com sobrevida e com os níveis
de CEA sérico, com diferença significante entre os
estádios morfofuncionais II e III. Foi possível
demonstrar que a curva de sobrevida no
estadiamento morfofuncional apresentou resultados semelhantes
aos encontrados no estadiamento TNM (figura 2). A
importância da incorporação de variáveis funcionais
na proposta de estadiamento pôde ser bem
demonstrada quando se verificou maior correlação entre o
nível sérico de CEA e o estadiamento morfofuncional
proposto (tabela 2).
Observa-se, à semelhança de outras
classificações, que o TNM detecta a extensão clínica da
doença avaliada no momento da excisão da lesão,
não considerando agressividade, poder de
disseminação, resultantes do genótipo do tumor. A análise indireta
da expressão de genes, pela detecção tecidual das
proteínas por eles codificadas, tal como o CEA, possibilita
a avaliação funcional da neoplasia relacionada ao
desenvolvimento, crescimento e disseminação do tumor.
Desta forma foi possível analisar a importância da
dinâmica celular funcional como fator relacionado ao
prognóstico da enfermidade, representando, em síntese, as
mutações a que as células cólicas foram
submetidas.20
As evidências encontradas no presente
estudo, sugerem que há dois mecanismos responsáveis
pelos níveis séricos do CEA no CCR. O primeiro
representado pela diferença de produção e excreção
nas subpopulações tumorais e perda da capacidade de
polarização do CEA (classificação morfofuncional);
o segundo, representado pela massa tumoral
produtora de antígeno e o grau de invasão na parede
intestinal (TNM). A possibilidade de analisar estes dois
mecanismos de forma conjunta, origina nova proposta
de estadiamento, útil na predição evolutiva da doença,
especialmente por se relacionar aos níveis séricos de CEA.
Os resultados encontrados no presente estudo, permitem concluir que o
estadiamento morfofuncional é uma estratégia válida para a
avaliação prognóstica dos pacientes com câncer
colorretal por considerar a dinâmica funcional da célula, além
de se relacionar com os níveis séricos do CEA.
ABSTRACT: The analysis of morphofunctions characteristics can be useful in the colorectal cancer evolution, especially if related to the serum carcinoembryonic antigen levels. The research of chromosomes and genes instability, as well as the alterations of tissue protein codified, makes attractive the possibility to use potentially valid functional factors as variables for the understanding of colorectal carcinoma prognosis. Objective: To consider classes based on morphologic and functional colorectal carcinoma characteristics, valuing serum carcinoembryonic antigen levels prognostic power. Method: Third-five patients in different stages of colorectal carcinoma underwent operations from 2001 to 2007. Serum CEA levels, histological grade, tissue CEA cell polarization capacity were analyzed. Colorectal carcinoma was classified according to TNM stages. The morphofunctional classification was determined by the combination between histological grade and antigen polarization, morphofunctional stages have been based in association between morphofunctional classification and stages TNM, by punctuation attributed to each one classification. The results had been analyzed by variance analysis, correlation test and survival analysis (Kaplan-Meier and Cox Model Regression), adopting p<0.05. Results: Morphofunctional stages survival curve resulted similar to the joined ones in stages TNM. It had relation between new classification proposed and patient survival time. They had observed relation among survival time, morphofunctional classification and serum carcinoembryonic antigen. Conclusion: Morphofunctional classification is valid for colorectal cancer patient's prognostic evaluation and is related with the serum CEA levels.
Key words: Carcinoembryonic antigen, Immunohistochemistry, Survival Analysis, Neoplasm Staging, Prognosis, Colorectal carcinoma.
REFERÊNCIAS
1. Pinho MSL. Estadiamento molecular do câncer
colorretal: O futuro se aproxima. Rev bras Coloproct
2005;25:279-84.
2. Boring CC, Squires TS, Tong T. Cancer statistics 1993.
CA Cancer J Clin 1993;43:7-26.
3. Miller SF, Knigth AR. The early detection of colorectal
cancer. Cancer 1977;40:945-9.
4. Stower MJ, Hardcastle JD. The results of 1115 patients
with colorectal cancer treated over an 8 years period in a
single hospital. Eur J Surg Oncol 1985;11:119-23.
5. Neves FJ, Mattos IE, Koifman RJ. Mortalidade por câncer
de cólon e reto nas capitais brasileiras no período
1980-1997. Arq Gastroenterol 2005;42:63-70.
6. Rich T, Gunderson LL, Lew R, Galdibini JJ, Cohen
AM, Donaldson G. Patterns of recurrence of rectal cancer
after potentially curative surgery. Cancer 1983; 52:1317-29.
7. Michelassi F, Vanucci L, Ayala JJ, Chappel R, Goldrerg
R, Block GE. Local recurrence after curative resection of
colorectal adenocarcinoma. Surgery 1990;108:787-93.
8. Kemeny N, Braun DWJr. Prognostic factors in
advanced colorectal carcinoma. Importance of lactic dehydrogenase
level, performance status, and white blood cell count. Am J
Med 1983; 74:786-96.
9. Ponz de Leon M, Sant M, Micheli A, Sacchetti C, Di
Gregorio C, Fante R, Zanghieri G, Melotti G, Gatta G. Clinical
and pathologic prognostic indicators in colorectal cancer.
A population-based study. Cancer 1992;69:626-35.
10. Sanfelippo PM, Beahrs OH. Factors in the prognosis
of adenocarcinoma of the colon and rectum. Arch
Surg 1972;104:401-6.
11. Cain AS, Longino LA. Carcinoma of the colon in children.
J Pediatr Surg.1970; 5:527-32.
12. Wolmark N, Wieand HS, Rockette HE, Fischer B, Glass
A, Lawrence W, Lerner N, Cruz AB, Volk H, Shibata H, Evans
J, Prager D. The prognostic significance of tumor location
and bowel obstruction in Dukes B and C colorectal cancer.
Findings from the NSABP clinical trials 1983;198:743-52.
13. Grinnel RS. The grading and prognosis of carcinoma of
the colon and rectum. Ann Surg 1939;109:500-33.
14. Dukes CE. The classification of cancer of the rectum. J
Pathol 1932;35:323-32.
15. Astler VB, Coller FA. The prognostic significance of
direct extension of carcinoma of the colon and rectum. Ann
Surg 1954;139:846-51.
16. Halvorsen TB, Sein E. Influence of mucinous components
on survival in colorectal adenocarcinomas: a multivariate
analysis. J Clin Pathol 1988;41:1068-72.
17. Martinez CAR, Priolli DG, Cardinalli IA, Piovesam H,
Pereira JA. Importância da correlação entre o padrão de
distribuição tecidual do antígeno carcinoembriônico e seus níveis
séricos no prognóstico do câncer colorretal. Estudo prospectivo
de 50 casos. Rev bras Coloproct 2004;24 (supl.1):90.
18. Knudsen JB, Nilsson T, Sprechler M, Johansen A,
Christensen N. Venous and nerve invasion as prognostic factors
in postoperative survival of patients with resectable cancer
of the rectum. Dis Colon Rectum 1983;26:613-17.
19. Phillips RK, Hittinger R, Blesowsky L, Fry JS, Fielding
LP. Large bowel cancer: surgical pathology and its relationship
to survival. Br J Surg 1984;71:604-10.
20. Kune GA, Kune S, Field B, White R, Brough W,
Schellemberger R, Watson LF. Survival in patients with large-bowel cancer.
A population-based investigation from Melbourne
Colorectal Cancer Study. Dis Colon Rectum 1990;33:938-46.
21. Pinho MSL. Estadiamento molecular do câncer colorretal:
O futuro se aproxima. Rev bras Coloproct 2005;25:279-84.
22. Gold P, Freedman SO. Demonstration of tumor-specific
antigens in human colonic carcinoma by immunological tolerance
and absorption techniques. J Exp Med 1965;121:439-62.
23. Tate H. Plasma CEA in the post-surgical monitoring
of colorectal carcinoma. Br J Cancer 1982;46:323-30.
24. Forones NM, Tanaka M. CEA and Ca 19-9 as
prognostic indexes in colorectal cancer.
Hepatogastroenteroly 1999;46:905-8.
25. Chapman MAS, Buckley D, Henson DB, Armitage
NC. Preoperative carcinoembryonic antigen is related to tumor
stage and long-term survival in colorectal cancer. Brit J
Cancer 1998;78:1346-9.
26. Costa CA, Macedo JLS, Reis PEG, Povoa C, Mendes
D, Cruz D. O valor do CEA no estadiamento do
adenocarcinoma colorretal. Rev Bras Cir 1996;86:171-3.
27. Solimene AC, Carneiro CRW, Melati I, Lopes JD.
Functional differences between two morphologically distinct
cell subpopulations within a human colorectal carcinoma cell
line. Braz J Med Biol Res 2001;34:653-61.
28. Hamada Y, Yamamura M, Hioki K, Yamamoto M, Nagura
H, Watanabe K. CEA distribuition pattern and the CEA levels
in the peripheral blood in patients with colorectal
carcinoma. Cancer 1985;55:136-41
29. Nathanson SD, Shultz L, Tilley B, Kambouris A.
Carcinomas of the colon and rectum: a comparative of
staging classifications. Am Surg 1986;52:428-33.
30. Gloeckler LA, SEER Cancer statistics review
1973-1991. USDHHS, PHS, NIH, NIH publication no. 1994;94:2789.
31. Martinez CAR, Priolli DG, Cardinalli IA, Piovesan H,
Pereira JA, Waisberg J, Margarido NF. Correlação entre o padrão
de expressão tecidual e os valores séricos do
antígeno carcinoembrionário em doentes com câncer colorretal. Rev
bras Coloproct 2006;26:41-53.
32. Chapman MAS, Buckley D, Henson DB, Armitage
NC. Preoperative carcinoembryonic antigen is related to tumor
stage and long-term survival in colorectal cancer. Brit J
Cancer 1998;78:1346-9.
33. Castells A, Bessa X, Daniels M, Ascaso C, Lacy A. Value
of postoperative surveillance after radical surgery for
colorectal cancer. Dis Colon Rectum 1998;41:714-24.
34. Pagé M, Dalifard I, Bertrand G, Bocquillon PG, Daver
A. Immunostaining of colorectal cancer with monoclonal
anti-CEA antibodies compared to serum and tumor CEA
content. Anticancer Res 1986;6:893-6.
35. Schoentag R, Williams V, Kuhns W. The distribuition of
blood group substance H and CEA in colorectal carcinoma.
Cancer 1984;53:503-9.
36. Chammas R, Novak EM. Mecanismos de invasão e
metástases em câncer colorretal. In: Rossi BM, Nakagawa WT,
Ferreira FO, Aguiar Junior S, Lopes A. Câncer de Cólon, Reto e
Ânus.1nd ed. São Paulo: Lemar & Tecmedd Editora; 2004. p.55-62.
37. Fantini J, Rognoni JB, Culouscou JM, Pommier G,
Marvaldi J, Tirard A. Induction of polarized apical expression
and vectorial release of carcinoembryonic antigen (CEA)
during the process of differentiation of HT29-D4 cells. J Cell
Physiol 1989;141:126-34.
38. Shirota K, Minassian H, Jothy S. Protein
G-gold immunoelectron microscopy of the colon carcinoma: the
effect of tumor differentiation of carcinoembryonic
antigen immunostaining. Exp Mol Pathol 1988;49:305-15.
39. Huitric E, Laumonier R, Burtin P, Von Kleist S, Chavonel
G. An optical and ultrastructural study of the localization
of carcinoembryonic antigen (CEA) in normal and
cancerous human rectocolonic mucosa. Lab Invest 1976;34:97-107.
40. Lorenzi M, Vindigni C, Manacci C, Tripodi SA, Iroatulam
A, Petrioli R, Franchini G. Histopathological and
prognostic evaluation of immunohistochemical findings in
colorectal cancer.Int J Biol Markers 1997;12:68-74.
41. Chiquillo Barber MT, Bort Marti I, Navarro Fos S,
Perez Bacete M, Esclapez Valero J, Gómez-Ferrer Bayo
F. Correlación entre niveles séricos de CEA preoperatorios
y tinción inmunohistoquímica del CEA en el carcinoma
colorrectal. Rev Esp Enferm Dig 1993;83:249-54.
42. Pihl E, McNaughtan J, Ward HA, Nairn
RC. Immunohistological patterns of carcinoembryonic antigen
in colorectal carcinoma. Correlation with staging and blood
levels. Pathology 1980;12:7-13.
43. Zeng Z, Cohen AM, Urmacher C. Usefulness
of carcinoembryonic antigen monitoring despite
normal preoperative values in node-positive colon cancer
patients. Dis Colon Rectum 1993;36:1063-8.
44. Moertel CG, Schutt AJ, Go VL. Carcinoembryonic
antigen test for recurrent colorectal carcinoma. Inadequacy for
early detection. JAMA 1978;239:1065-6.
45. Waisberg J, Landman G, Cha ASH, Henriques AC,
Gaspar HA, Speranzini MB. Padrão da distribuição tecidual do
CEA no carcinoma colo-retal: relação com o nível sérico do CEA
e classificação de Dukes. Rev bras Coloproct 2002;22:20-6.
46. Steele G Jr., Ellenberg S, Ramming K, O'Connel M,
Moertel C, Lessner H. CEA monitoring among patients in
multi-institucional adjuvant G.I. Therapy protocols. Ann
Surg 1982;196:162-69.
47. Sunouchi K, Machinami R, Mori M, Namiki K, Hattori
S, Murata Y, Tsuchiya T, Mizuno H, Tadokoro M.
Clinical impact of carcinoembrionic antigen messenger ribonucleic
acid expression in tumor-draining vein blood on postoperative
liver metastasis in patients with colorectal carcinoma: a
prospective cohort study. Dis Colon Rectum 2003;46:467-73.
48. UICC Committee on TNM Classification. Malignant
tumors of oesophagus, stomach, colon and rectum. Geneve:
UICC; 1966.
Endereço para correspondência:
Denise Gonçalves Priolli
Rua São Vicente 614 - Bairro Jardim Paulista
Atibaia - SP
12947-390
Fone/fax: (11)4412-7730
E-mail: depriolli@terra.com.br
Recebido em 10/09/2007
Aceito para publicação em 23/10/2007
Trabalho realizado no Programa de Pós-graduação em Ciências da Saúde e Disciplina de Anatomia Patológica do Curso de Medicina, da Universidade São Francisco, Bragança Paulista, São Paulo, Brasil.