ARTIGOS ORIGINAIS
FATORES PROGNÓSTICOS E SOBREVIDA NO ADENOCARCINOMA PRIMÁRIO DE RETO
Prognostic Factors and Survival in Primary Rectal Adenocarcinoma
Heloisa Guedes MÜssnich1, Luis Fernando Moreira2, Pedro Gus3, Marcelo Pimentel4, Tatiana Simon4, Marcelo Bellon dos Santos4
1 Coloproctologista, Mestranda do Curso de Pós-Graduação em Medicina: Cirurgia, Faculdade de Medicina/Universidade Federal do Rio Grande do Sul (FAMED/UFRGS), Porto Alegre, RS; 2 Co-orientador, Professor Doutor do Curso de Pós-Graduação em Medicina: Cirurgia FAMED/UFRGS, Porto Alegre, RS; 3 Orientador, Professor Titular, Livre-docente em Coloproctologia; 4 Médico, Bolsista de Iniciação científica, FAMED/UFRGS, Porto Alegre, RS.
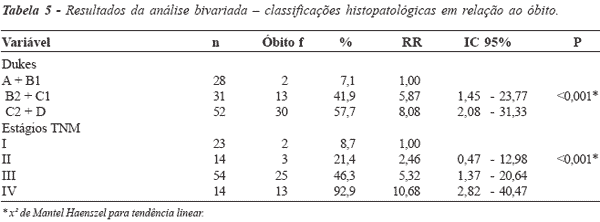
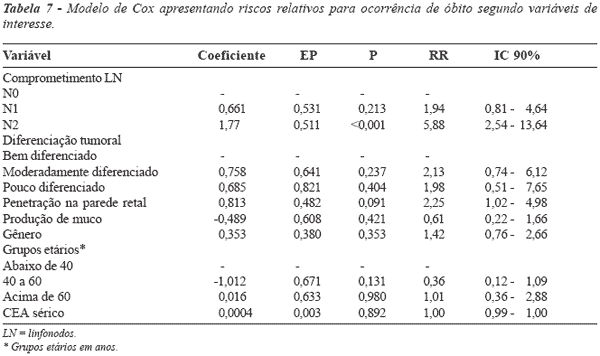
RESUMO: Objetivo: Avaliar a sobrevida e fatores clínico-patológicos relacionados ao adenocarcinoma de reto. Metodologia: Foram revisados 112 prontuários de pacientes com adenocarcinoma de reto quanto a: idade, sexo, antígeno carcino-embriônico, curabilidade da cirurgia, seguimento, recidiva, sobrevida e histopatologia do tumor. Para análise da sobrevida, utilizou-se o método de Kaplan-Meyer. Nas análises bivariada e estratificada, P <0,05 foi significativo. No modelo multivariado, utilizou-se um IC de 90%. Resultados: O seguimento mediano foi de 35,27 meses (14,5 _ 57,63). A sobrevida em 5 anos foi de 51%. Sessenta e quatro pacientes (57%) apresentaram recidiva; 45 (40%) faleceram da neoplasia; 68% dos tumores estendiam-se até os tecidos perirretais; e 67 pacientes tinham linfonodos positivos (30% em cada, N1 e N2). Quatorze pacientes eram estágio D; 55, C1 e C2; 15, B2; e 28, B1 e A. O risco de óbito aumentou entre os casos com: estágios avançados, tumores mais invasivos e menos diferenciados, envolvimento linfonodal (N2>N1) e recidiva. A classificação de Dukes e a diferenciação tumoral foram fatores prognósticos independentes, bem como a penetração do tumor na parede retal e o comprometimento linfonodal, quando excluída a classificação histopatológica. Conclusão: Além da diferenciação tumoral, os fatores prognósticos identificados correspondem aos níveis dos sistemas de estadiamento vigentes.
Descritores: Adenocarcinoma de reto, fatores prognósticos, classificaçăo histopatológica, recidiva, sobrevida.
INTRODUÇÃO
O câncer colorretal é a terceira neoplasia
mais freqüente no mundo
ocidental(1), sendo que o reto é atingido em 30 a 57% dos
casos(2,3). Mais de 50% dos pacientes têm tumores avançados no momento do
diagnóstico, e a sobrevida em 5 anos se mantém em
torno de 50% em todo o mundo(4-7). Embora um
grande número de estudos tenha avaliado vários
parâmetros clínicos, patológicos e moleculares em relação ao
prognóstico, até o momento, o estadiamento
clinicopatológico das lesões, obtido do espécime cirúrgico na
ressecção do tumor primário, constitui a informação
prognóstica mais importante disponível para esses
pacientes(8-12).
O presente estudo tem como objetivo avaliar a sobrevida e os fatores clinicopatológicos
relacionados aos tumores de reto em nosso meio.
PACIENTES E MÉTODOS
Os prontuários de 112 pacientes com adenocarcinoma primário e único de reto médio ou
distal (de 3 a 12 cm da margem anal) submetidos à
cirurgia eletiva no Serviço de Coloproctologia do Hospital
de Clínicas de Porto Alegre, no período de 1988 a
1995, foram revisados retrospectivamente quanto a:
idade, sexo, antígeno carcino-embriônico (CEA)
pré-operatório, seguimento (até o término da coleta de
dados, em 1998), recidiva locorregional ou à
distância, sobrevida e histopatologia do tumor (diferenciação
celular, grau de penetração na parede,
comprometimento linfonodal, produção de muco e comprometimento
de margens cirúrgicas). Foram excluídos os casos
com lesões sincrônicas, metacrônicas ou simultâneas
de outros órgãos, com doenças intestinais associadas
ou tratamentos fora da rotina do referido Serviço
(retocolite ulcerativa, radioterapia pré-operatória, cirurgia
sem ressecção intestinal ou realizada em outro serviço).
Os tumores foram classificados, a partir dos
laudos anatomopatológicos do Serviço de Patologia do
referido hospital, segundo o sistema de estadiamento
de Dukes modificado por Astler-Coller, e comparados
ao sistema TNM.
O seguimento dos pacientes foi avaliado através dos exames de estadiamento disponíveis nos
prontuários (radiografia de tórax, ecografia ou
tomografia abdominal, dosagem sérica de CEA e endoscopia
digestiva baixa - retossigmoidoscopia ou
colonoscopia), ou através do contato com os próprios pacientes
ou seus familiares. Os pacientes com doença
metastática no momento do diagnóstico foram excluídos da
análise de recidiva.
Para permitir tratamento estatístico
adequado, em virtude do número reduzido de pacientes em
alguns grupos, os estágios da classificação de Dukes
modificada por Astler-Coller foram distribuídos em
subgrupos, de acordo com o prognóstico e a perspectiva
terapêutica atual: subgrupos 1 (A e B1), 2 (B2 e C1) e 3 (C2
e D). O coeficiente de correlação de Kendall foi
utilizado para comparação dos sistemas de estadiamento.
A sobrevida foi avaliada pelo método de
Kaplan-Meyer. Nas análises bivariada e estratificada, um valor de
P <0,05 foi considerado significativo. No
modelo multivariado, utilizou-se um IC de 90% (=0,10).
RESULTADOS
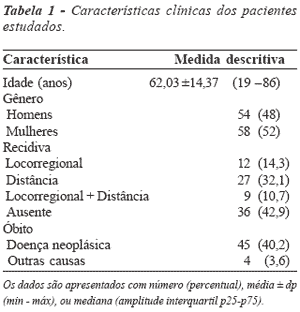
As características clínicas dos pacientes
estão resumidas na Tabela 1. O CEA pré-operatório foi
avaliado em 78,6% dos casos, e variou de 0,4ng/dl a
658ng/dl, com mediana de 4,75 (2,20 _ 13,45). A
amputação abdominoperineal de reto foi realizada em 63
pacientes (56,3%), e a retossigmoidectomia, com ou
sem anastomose, no restante dos casos. Sessenta e
quatro pacientes (57%) apresentaram recidiva tumoral,
sendo 14,3% locorregional, 32,1% à distância e 10,7%
simultâneas. O tratamento complementar adjuvante
foi realizado em 19,3% dos casos, e o paliativo, em
32 pacientes (28,6%).
 |
 |
Figura 1 - Curva de sobrevida. |
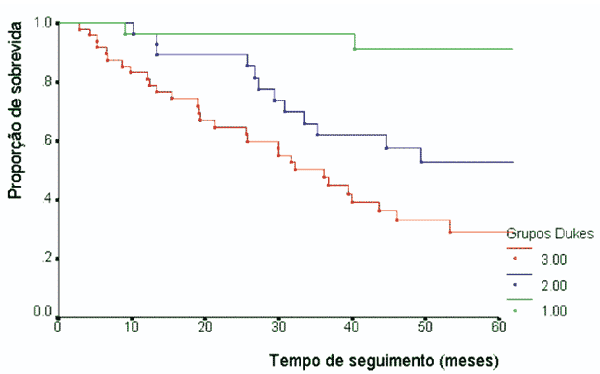 |
Figura 2 - Curvas de sobrevida pelos subgrupos de Dukes.
(1= A+B1; 2= B2+C1; 3= C2+D) |
 |
 |
 |
 |
 |
 |
DISCUSSÃO
A média de idade e a distribuição por
sexo mantiveram as características anteriormente
descritas por Rosito et al.(13),e correspondem à distribuição
usual na literatura(2,14,15). Embora não tenham sido
relacionados à recorrência local em um estudo
multicêntrico(16), outros autores encontraram valor prognóstico
independente para o sexo, com pior sobrevida entre os
indivíduos do sexo
masculino(12,17-19). Em nossa
experiência, nem a idade nem o sexo mostraram ser fatores
prognósticos independentes para a sobrevida. O
possível efeito protetor da faixa etária de 40 a 60 anos pode
não corresponder à realidade. No entanto, Nan et
al.(20) encontraram pior sobrevida no grupo de idosos
acima de 75 anos portadores de câncer colorretal, tendo
relacionado o achado ao diagnóstico tardio. Da
mesma forma, também atribuindo ao retardo no
diagnóstico, com 66% dos pacientes em estágios III e IV da
doença _ porém associado com tumores mais agressivos,
_ o grupo etário mais jovem (abaixo de 40 anos)
também tem sido relacionado a piores
prognósticos(2,12,21,22) , com altas taxas de mortalidade (25% num seguimento
médio de 26 meses)(23). No entanto, parece que esse
efeito é minimizado quando a análise de sobrevida é
ajustada de acordo com o estágio do
tumor(12). Nesta casuística, necessitaríamos de um número maior
de pacientes para confirmar tal achado.
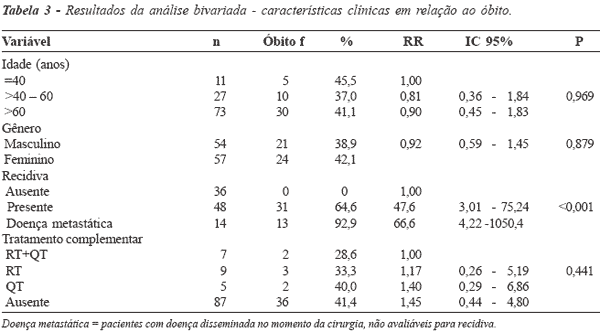
No momento da cirurgia, 13% dos pacientes apresentavam metástases à distância. O índice de
cirurgias não-curativas foi de 22,5%, considerando
esses casos com doença metastática (n=14) e os
pacientes com comprometimento do limite radial das
margens cirúrgicas (n=15; alguns casos
apresentaram envolvimento simultâneo). Estes casos são
invariavelmente relacionados a piores
prognósticos(8,12,24,25), fato este também observado nesta série. Em outras
revisões, em torno de 25% dos pacientes já
apresentavam envolvimento metastático à distância no momento
do diagnóstico(26).
O índice de recidiva locorregional isolada
foi de 14%. Outros 10,7% desenvolveram recidiva locorregional associada a metástases à
distância, totalizando 24,7% de recorrência tumoral local.
Pinho et al.(7), em um levantamento prospectivo de 97
pacientes com câncer colorretal submetidos à cirurgia
com intenção curativa, encontraram um percentual de
12,5%. Na casuística anterior do Serviço, a
recidiva locorregional ocorreu em 20% dos
casos(13). As taxas de recorrência local, no mundo, variam de 20
a 45%(10,16,27-29). Sabe-se que os melhores índices
obtidos até hoje foram de 2,6% com a ressecção total
do mesorreto(10,30). Resultados semelhantes
(3,8%(31) e 4,7%(32)) têm sido obtidos em nosso meio com o
auxílio de terapia complementar pré-operatória. Os casos
de recidiva, em nossa casuística, tiveram uma
mortalidade significativamente maior. Na literatura, a
sobrevida em 5 anos após ressecção da recidiva não chega
a 30%, comparável aos casos de doença
metastática(33). A ocorrência de recidiva aumentou
progressivamente à medida que avançaram os estágios
histopatológicos da doença. Esse achado também foi observado
por outros autores(16). Na análise estratificada, no
entanto, somente no subgrupo de Dukes de pior prognóstico,
os pacientes com metástases à distância e recidiva
apresentaram risco significativo de óbito em relação
àqueles sem recidiva.
No período de seguimento (mediano de
35,27 meses), 44% dos pacientes foram a óbito, sendo
40% da mortalidade relacionada à neoplasia. Esses
dados correspondem aos achados da
literatura(2,8,17,34). O tempo mediano de sobrevida relacionada à neoplasia
foi de 71,8 meses. A sobrevida global em 5 anos foi
de 51%. A proporção de sobrevida piorou
significativamente à medida que avançaram os estágios de
Dukes (subgrupo 1, 91%; subgrupo 2, 57%; e subgrupo 3,
39%) _ no período de 40 meses, tendo em vista que o
primeiro grupo não alcançou 50% de mortalidade no
tempo mediano de sobrevida geral (71,83 meses). Pinho
et al.(7) encontraram uma sobrevida em 5 anos de
52%, sendo 89% para pacientes estágio 1, 70% para
pacientes estágio 2 e 20% para os pacientes estágio 3.
No relato de Norstein et al.(16), a sobrevida em 5 anos
foi de 55,2%, também piorando quanto mais avançado
o estágio da doença (77% Dukes A; 48% Dukes B;
e 35% Dukes C). Da mesma forma, Hermanek et
al.(27) observaram uma sobrevida relacionada à
doença neoplásica de 66%, com uma variabilidade
proporcional aos estágios de TNM: estágio I, de 89 a 100%
entre os centros; estágio II, de 58 a 92%; e estágio III,
de 13 a 69%. Nan et al.(20) também encontraram
sobrevida relacionada aos estágios de Dukes, que
demonstrou ser fator prognóstico independente na
análise multivariada(20).
O valor da dosagem pré-operatória de
CEA sérico na avaliação prognóstica dos pacientes tem
sido amplamente discutido(8,12,24,35). Embora níveis
elevados estejam sendo relacionados, a maior risco de
recidiva e piora na sobrevida por alguns
autores(12,17,36), essa variável não foi identificada como um fator
prognóstico independente na análise
multivariada(17). Contudo, tem sido postulado que uma dosagem
pré-operatória elevada pode estar relacionada a recorrência e
piora na sobrevida(12). Atualmente, a dosagem
pré-operatória de CEA tem sido usada como referência para
o seguimento do paciente(17). O uso da dosagem
isolada de CEA para monitorar resposta terapêutica não
está sendo recomendado(8), mas a AJCC recomenda a
inclusão desta característica em uma subcategoria
do sistema TNM, como marcador
prognóstico(24,35). Em nosso estudo, a dosagem sérica do CEA
pré-operatório não demonstrou impacto na sobrevida dos
pacientes, embora se possa considerar que o tamanho
amostral seja modesto para esta avaliação.
O adenocarcinoma moderadamente diferenciado foi o tipo histológico mais freqüente, em 73%
dos casos, seguido de 18% de lesões bem diferenciadas
e 9 casos de adenocarcinoma pouco diferenciado
(8%). Esses percentuais são semelhantes aos
encontrados na literatura (15,37), e aos observados previamente
em nosso Serviço (20% bem diferenciados, 65%
moderadamente diferenciados e 3,4%, pouco diferenciados
_ 11,6% foram considerados
indiferenciados)(13). O risco de óbito foi três vezes maior entre os tumores
menos diferenciados (P= 0,009), na análise
bivariada. Apesar disso, a análise estratificada não detectou
efeito da diferenciação tumoral, possivelmente porque
o tamanho amostral de cada subgrupo era pequeno.
Já no modelo de Cox, esse efeito se manifestou em
relação ao estrato dos tumores pouco diferenciados,
quando comparado aos bem diferenciados, sendo
independente do efeito dos estágios de Dukes. Os
tumores menos diferenciados têm sido diretamente
relacionados à recorrência local(38)
e à piora na
sobrevida(18-20). Contudo, resultados conflitantes vêm sendo
encontrados, possivelmente pelos complexos critérios de
avaliação, que não são
padronizados(18,20,34). Entre 24 estudos realizados com análise multivariada, 10
demonstraram valor prognóstico independente, mas, em
comparação com o estágio do tumor, o grau de
diferenciação não acrescentou nenhuma vantagem
significativa na previsão da
sobrevida(17). Em outro estudo, foi considerado fator prognóstico independente,
juntamente com o estágio do
tumor(20).
Em 18 casos, os tumores eram produtores de muco. Essa característica não apresentou
influência significativa na sobrevida, confirmando os achados
de Rawet(18) e Ratto et
al.(17) Contudo, a análise histopatológica de um tumor demonstrando
áreas mucinosas ou células em anel de sinete tem levado
à identificação de tumores mais agressivos, com
pior potencial prognóstico(12). No entanto, a piora do
prognóstico parece ter sido atribuída ao estágio
avançado da doença(17).
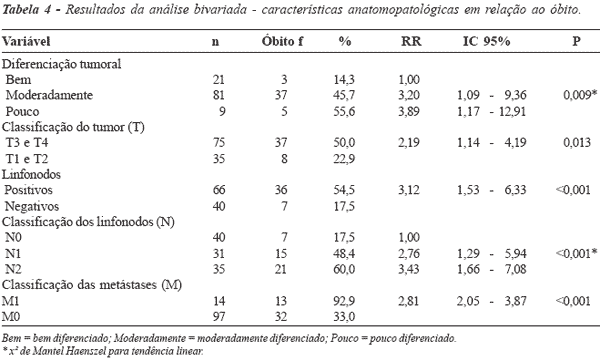
A maior parte das lesões estendia-se até
os tecidos perirretais (68,2%). Os pacientes com
tumores de maior grau de penetração na parede (T3 e T4)
apresentaram o dobro do risco de óbito em relação
aos menos avançados (T1 e T2). O grau de invasão
tumoral provou ter relação direta com o
prognóstico(24,25). Cinqüenta e cinco pacientes pertenciam aos estágios C1
e C2 de Dukes modificado por Astler-Coller (TNM
III). Pouco mais de 20% dos casos ficaram
classificados nos estágios mais precoces. Essa observação vai
ao encontro da experiência comum de diagnósticos
tardios(22,23), e deve reforçar a importância dos
programas de prevenção e detecção precoces, uma vez que
os tumores de reto médio e distal encontram-se
acessíveis ao diagnóstico e ao estadiamento em exame
clínico de rotina(39).
A média (dp) de linfonodos isolados da
peça cirúrgica foi de 14,4 (±10,25) linfonodos. A
recomendação da AJCC(8) é de que no mínimo 12
linfonodos sejam isolados da peça cirúrgica para a
determinação confiável do nível de envolvimento
linfonodal(8), o que tem demonstrado influência negativa no
prognóstico(12,20,24,40,41). O número de linfonodos positivos
variou de 1 a 39, com média (dp) de 6,8 (±7,9)
linfonodos, correspondendo a mais de 60% dos casos
com envolvimento linfonodal. Os pacientes com
linfonodos positivos apresentaram risco de óbito três vezes
maior, sendo que a quantificação dos linfonodos
comprometidos demonstrou valor prognóstico significativo,
corroborando achados de outros autores(15,17,18,34,41)
. Cinco estudos investigaram o número de linfonodos com
comprometimento metastático para
determinação prognóstica; apenas dois destes mostraram
valor preditivo adequado para este parâmetro no
prognóstico(17). Esses dados contrastantes são
possivelmente conseqüentes às variações entre técnicas
histológicas, que podem subestadiar os tumores. A AJCC
recomenda inclusão do envolvimento linfonodal metastático
na categoria I, de fatores definidamente influentes no
prognóstico(24).
CONCLUSÕES
Os fatores que demonstraram efeito
prognóstico independente nesta casuística foram:
diferenciação tumoral, grau de penetração do tumor na parede
e comprometimento linfonodal, além da
classificação histopatológica propriamente dita.
A sobrevida relacionada à neoplasia dos
pacientes com tumor de reto médio e distal foi de 51%
em cinco anos. Observou-se uma piora significativa
da recidiva tumoral e da sobrevida à medida que
avançaram os estágios da doença. Os achados deste
estudo estão de acordo com a literatura: apesar das
limitações, os níveis dos sistemas de
classificação histopatológica dos tumores ainda são os critérios
prognósticos disponíveis. Estas conclusões devem ser
reforçadas em estudos com maior número de pacientes.
AGRADECIMENTO
Os autores agradecem a Mario Wagner, PhD. pelo auxílio na análise estatística.
ABSTRACT: The objective of this study was to evaluate survival and clinicopathological factors in rectal adenocarcinoma, the records of 112 patients were reviewed for: age, gender, serum level of CEA, surgery curability, follow-up, recurrence, survival and tumor histopathology. Kaplan-Meyer curves were used to analyze survival. Statistical significance in bivariate and stratified analysis was set at P < 0.05. In the multivariate model, a 90% confidence interval was considered significant. Median follow-up was 35 (14 - 57) months. Five-year survival rate was 51%. Sixty-four patients (57%) had recurrence; 45 (40%) died from neoplasia, 68% tumors extended to perirectal tissues and 67 had positive lymph nodes (30% each, N1 and N2). Fourteen patients were Dukes D stage; 55 were C1 and C2; 15 were B2; and 28 were B1 and A. Death increased significantly with tumor progression stages (P<0.001), tumor depth (P=0.013) and grade (P=0.009), lymph node involvement (N2>N1, P<0.001) and recurrence (P<0.001). Independent prognostic factors were Dukes stages and tumor grade (P=0.089), as well as depth of invasion and lymph node involvement when Dukes staging was excluded (P=0.091 and <0.001). Besides tumor grade, the prognostic factors identified meet classification levels in current staging systems.
Key words: Rectal adenocarcinoma, prognostic factors, histopathological staging, recurrence, survival.
REFERÊNCIAS
1. Ky AJ, Sung MW, Milsom JW. Research in colon and
rectal cancer, with an emphasis on surgical progress. Dis
Colon Rectum 1999; 42(11): 1369-1380.
2. Williams NS. Colorectal cancer:
epidemiology, aetiology, pathology, clinical features and
diagnosis. In: Keighley MR, Williams NS, eds. Surgery of
the anus, rectum and colon. London: WB Saunders;
1993. p. 830-885.
3. Santos JCM Jr. Tratamento coadjuvante do câncer do reto: I
- Radioterapia pré-operatória. Rev Bras Coloproct 1997;
17(1): 69-73.
4. Wilmink AB. Overview of the epidemiology of
colorectal cancer. Dis Colon Rectum 1997; 40(4): 483-493.
5. European School of Oncology. Task Force Preview,
Geneva, Switzerland. Issue 2, Sept 1997.
6. Brasil, Ministério da Saúde, Instituto Nacional do
Câncer, Coordenadoria de Programas de Controle do Câncer. O
problema do câncer no Brasil.
4ª ed. Rio de Janeiro: INCa/ Pro- Onco; 1997.
7. Pinho MSL, Ferreira LC, Kleinubing Jr. H. Tratamento
cirúrgico do câncer colorretal: resultados a longo prazo e análise
da qualidade. Rev Bras Coloproct 2006; 26(4): 422-429.
8. National Cancer Institute, PDQ. Rectal Cancer. 2007;
1-27. Available: http://www.cancer.gov
9. Pinho MSL. Marcadores moleculares como fatores
prognósticos do câncer colorretal. Rev Bras Coloproct 1999; 19
(2): 130-132.
10. MacFarlane JK, Ryall RD, Heald RJ. Mesorectal excision
for rectal cancer. Lancet 1993; 341(8843): 457-460.
11. Macdonald JS. Adjuvant therapy of colon cancer. CA
Cancer J Clin 1999; 49(4): 202-219.
12. Department of pathology, SGPGIMS. Prognostic
factors predicting outcome in colorectal cancers. On-line
seminars and tutorials. Lucknow, India. 2007; 1-6. Available:
http://www.sgpgi.ac.in/path/seminars.
13. Rosito MA, Müssnich JFX, Gus PG, Weindorfer M,
Schaefer LG, Pinheiro PM. Amputação abdomino-perineal
em adenocarcinoma de reto. II levantamento do HCPA.
Rev AMRIGS 1995; 39: 200-204.
14. Dias GB, Bauermann FB, Linhares EL, Mercado C,
Moreira LF. Estudo retrospectivo do índice de mortalidade por
câncer de cólon e de reto em Porto Alegre e no Rio Grande do
Sul. Proc XV JACAD 1997; 15: TL038-29.
15. Gordon PH. Malignant neoplasms of the colon. In:
Gordon PH, Nivatvongs S, eds. Principles and practice of surgery
for the colon, rectum and anus. St. Louis: Quality Medical;
1992. p. 501-565.
16. Norstein J, Langmark F. Results of rectal cancer treatment:
a national experience. In: Søreide O, Norstein J, eds.
Rectal cancer surgery. Optimisation - Standardisation
- Documentation. Oslo: Springer; 1997. p. 17-28.
17. Ratto C, Sofo L, Ippoliti M, Merico M, Doglietto GB,
Crucitti F. Prognostic factors in colorectal cancer: literature review
for clinical application. Dis Colon Rectum 1998; 41(8): 1033-1049.
18. Rawet V. Carcinoma colorretal: estadiamento e
parâmetros prognósticos [tese]. São Paulo: Universidade de São
Paulo; 1998.
19. Bokey EL, Chapuis PH, Dent OF, Newland RC, Koorey
SG, Zelas PJ, et al. Factors affecting survival after excision of
the rectum for cancer: a multivariate analysis. Dis Colon
Rectum 1997; 40(1): 3-10.
20. Nan KJ, Qin HX, Yang G. Prognostic factors in 165
elderly colorectal cancer patients. World J Gastroenterol. 2003;
9(10): 2207-2210.
21. Jessup JM, Menck HR, Fremgen A, Winchester
DP. Diagnosing colorectal carcinoma: clinical and
molecular approaches. CA Cancer J Clin 1997; 47(2): 70-92.
22. Carneiro Neto JD, Barreto JBP, Freitas NS, Queiroz
MA. Câncer colorretal: características clínicas e
anatomopatológicas em pacientes com idade inferior a 40 anos. Rev Bras
Coloproct, 2006; 26(4): 430-435.
23. Monteiro EP, Salem JB, Taglietti EM, Albuquerque IC,
Formiga GJS. Neoplasia colorretal até 40 anos _ experiência
em cinco anos. Rev Bras Coloproct. 2006; 26(2):156-161.
24. Compton CC, Fielding LP, Burgart LJ, Conley B, Cooper
HS, Hamilton SR, et al. Prognostic factors in colorectal
cancer. Arch Pathol Lab Med. 2000; 124(7): 979-994.
25. Wood CB, Gillis CR, Hole D, Malcolm AJ, Blumgart
LH. Local tumour invasion as a prognostic factor in
colorectal cancer. Br J Surg.1981; 68(5): 326-328.
26. Santos JCM Jr. Tratamento coadjuvante do câncer do reto:
II - Quimioterapia. Rev Bras Coloproct 1997; 17(2): 143-149.
27. Hermanek P. Impact of surgeon's technique on outcome
after treatment of rectal carcinoma. Dis Colon Rectum 1999;
42(5): 559-562.
28. Moriya Y, Hojo K, Sawada T, Koyama Y. Significance of
lateral node dissection for advanced rectal carcinoma at or
below the peritoneal reflection. Dis Colon Rectum 1989; 32(4):
307-315.
29. Moreira LF, Hizuta H, Iwagaki H, Tanaka N, Orita K.
Lateral lymph node dissection for rectal carcinoma below the
peritoneal reflection. Br J Surg 1994; 81(2): 293-296.
30. Heald RJ, Smedh RK, Kald A, Sexton R, Moran
BJ. Abdominoperineal excision of the rectum - an
endangered operation. Norman Nigro Lectureship. Dis Colon
Rectum 1997; 40(7): 747-751.
31. Reis Neto JA, Cordeiro F, Reis JA Jr, Kagohara O,
Simões Neto J. Laparoscopic total mesorectum excision. In: Reis
Neto JA, ed. New trends in coloproctology. Campinas:
Revinter; 2000. p. 497-504.
32. Habr-Gama A, Souza PM, Ribeiro U Jr., Campos F, Sousa
AH Jr., Nadalin W, Gansl R, et al. Low rectal cancer: impact of
pre-operative radiation and chemotherapy on surgical
treatment. "Hospital das Clínicas" of the University of São Paulo
Medical School experience. In: Reis Neto JA, ed. New trends
in coloproctology. Campinas: Revinter; 2000. p. 423-429.
33. Bozzetti F, Bertario L, Rossetti C, Gennari L, Andreola
S, Baratti D, et al. Surgical treatment of locally recurrent
rectal carcinoma. Dis Colon Rectum 1997; 40(12): 1421-1424.
34. Søreide O, Norstein J, Fielding P, Silen W.
International standardization and documentation of the treatment of
rectal cancer. In: Søreide O, Norstein J, eds. Rectal cancer
surgery. Optimisation - Standardisation - Documentation.
Oslo: Springer; 1997. p. 405-446.
35. Compton C, Fenoglio-Preiser CM, Pettigrew N, Fielding
LP. American Joint Committee on Cancer Prognostic
factors consensus conference: Colorectal Working Group.
Cancer 2000; 88(7): 1739-1757.
36. Kim JC, Han MS, Lee HK, Kim WS, Park SK, Park KC, et
al. Distribution of carcinoembryonic antigen and biologic
behavior in colorectal carcinoma. Dis Colon Rectum 1999;
42(5):640-648.
37. Mulcahy HE, Toner M, Patchett SE, Daly L,
O´Donoghue DP. Identifying stage B colorectal cancer patients at high
risk of tumor recurrence and death. Dis Colon Rectum 1997;
40(3): 326-331.
38. Reis Neto JA, Quilici FA, Cordeiro F, Ciquini S, Reis JA
Jr. Pre-operative radiotherapy in rectal cancer: evaluation
of irradiation effects on cellular undifferentiation and its
influence on prognosis. Hepatogastroenterology 1999; 46(29):
2825-2830.
39. Jucá MJ, Matos D, D'Ippolito G. Estudo da validação
do exame digital do reto no estadiamento clínico
pré-operatório dos adenocarcinomas tocáveis de reto. Rev Bras
Coloproct 1999; 19(4):248-258.
40. Chok KS, Law WL. Prognostic factors affecting survival
and recurrence of patients with pT1 and pT2 colorectal
cancer. World J Surg. 2007; 31(7): 1485-90. Epub 2007 May 18.
41. Hetnal M, Malecki K, Korzeniowski S, Zemelka
T. Postoperative chemoradiotherapy in patients with
rectal cancer, prognostic factors for disease control and survival.
J Clin Oncol. 2006; 24(18S): 13575.
Endereço para correspondência:
Heloisa Guedes Müssnich
Rua Ramiro Barcelos, 910/ conj. 1001
CEP 90035-001 - Porto Alegre - RS - Brasil
Fone/Fax: (51) 3311-7608
E-mail: lolomuss@brturbo.com.br
Recebido em 07/11/2007
Aceito para publicação em 22/01/2008
Trabalho realizado no hospital das Clínicas de Porto Alegre - Rio Grande do Sul - Brasil.