ARTIGOS ORIGINAIS
OS BENEFÍCIOS DA RESSECÇĂO ANTERIOR BAIXA EM MONOBLOCO PARA O CÂNCER DE OVÁRIO AVANÇADO: DEZ ANOS DE EXPERIĘNCIA EM UM ÚNICO CENTRO TERCIÁRIO
The Benefits of Low Anterior in Bloc Resection for Advanced Ovarian Cancer: Ten-Year Experience in a Single Tertiary Center
Sergio Renato Pais Costa1; Renato Arioni Lupinacci2
1 Especialista em Cancerologia Cirúrgica e Cirurgia do Aparelho Digestivo, Assistente do Serviço de Cirurgia Geral e Oncocirurgia do Hospital do Servidor Público Estadual de São Paulo - "Francisco Morato de Oliveira", Mestre em Cirurgia pela Universidade Federal de São Paulo - UNIFESP-EPM, São Paulo, Brasil; 2 Especialista em Coloproctologia, Diretor do Serviço de Cirurgia Geral e Oncocirurgia do Hospital do Servidor Público Estadual de São Paulo - "Francisco Morato de Oliveira", Doutor em Cirurgia pela Universidade Federal de São Paulo - UNIFESP-EPM, São Paulo, Brasil.
RESUMO: Introdução - A pedra angular do tratamento do câncer epitelial de ovário tem sido a associação da cirurgia citorredutora aliada à quimioterapia com platina. Quando essa neoplasia invade órgãos pélvicos adjacentes somente uma ressecção pélvica em monobloco pode levar a uma citorredução ótima. Objetivo - O objetivo do presente estudo foi acessar a segurança, a eficácia e o impacto na sobrevida da ressecção anterior baixa em monobloco para o câncer epitelial do ovário avançado. Métodos - Os dados completos de 19 pacientes que foram submetidos a esse tipo de operação para tratamento de câncer de ovário avançado entre Janeiro de 1996 a Junho de 2006 foram analisados. A mediana de idade foi de 58 anos (24-77). Em todas as cirurgias a doença residual foi menos do que 1 cm. Resultados - A mortalidade pós-operatória foi de 5% (n=1) enquanto a morbidade foi de 26,3 % (n=5). A sobrevida global em três anos foi de 76,47 % enquanto a mediana foi de 42 meses. Conclusões - A ressecção anterior baixa em monobloco não deve ser um obstáculo quando uma citorredução ótima é necessária. Em que pese sua alta morbidade, sua mortalidade é aceitável. O controle da doença em longo prazo pode ser atingido com esta prática.
Descritores: Exenteraçăo Pélvica, Câncer de Ovário, Morbidade, Mortalidade, Resultados do Tratamento.
INTRODUÇĂO
Aproximadamente 14,300 mulheres faleceram devido ao câncer de ovário em 2003, nos Estados
Unidos. Neste país, esta neoplasia representa a
principal causa de morte por câncer ginecológico. Em
linhas gerais, o câncer de ovário corresponde
respectivamente a 4% de todos os diagnósticos de câncer e cerca
de 5% de todos os óbitos por câncer. Em estádios
precoces é freqüentemente curável. Infelizmente, 60-70
% das pacientes apresentam-se em um estádio
avançado no momento de seu diagnóstico. A despeito do fato
de que a maioria das pacientes responde (80%)
inicialmente a quimioterapia, a maior parte sucumbe em
virtude da enfermidade. Os índices de sobrevida
global em cinco anos nos estádios avançados têm se
situado em torno de 10 %. Quando um tumor de ovário
avançado é descoberto durante a avaliação
intra-operatória, a conduta padronizada é um adequado
estadiamento cirúrgico associado a uma citorredução agressiva.
A citorredução refere-se à remoção de toda doença
possível. Enquanto que para a maioria dos tumores
sólidos, a ressecção cirúrgica agressiva somente se
justifica quando todo tumor pode ser removido
oferecendo uma cirurgia potencialmente curativa. Ao
contrário, para o câncer de ovário, a citorredução cirúrgica
quando a doença residual é menor que 1cm (citorredução
ótima) pode oferecer maiores índices de resposta
à quimioterapia, intervalos mais longos sem
progressão da doença e aumento na mediana de
sobrevida.1- 4
Tanto a definição de citorredução ótima
quanto a porcentagem de pacientes em estádios
avançados em que possa ser realizada essa abordagem, tem
variado amplamente na literatura. A definição
de citorredução ótima tem variado desde doença não
visível até 0,5 ou 1 cm de doença residual.
A porcentagem de pacientes em estádios
clínicos III-IV que podem ser submetidos a
uma citorredução ótima tem variado de 25% a 75%
dos casos. Desta maneira, a citorredução ótima não
pode ser atingida em uma proporção significativa das
doentes, principalmente nos tumores avançados. Por
sua vez, quando esses tumores invadem estruturas
pélvicas adjacentes (peritônio pélvico, fundo de saco,
bexiga, reto e cólon sigmóide) para se atingir uma
citorredução ótima, a solução tática é a realização de uma
ressecção anterior baixa associada a uma ressecção em
monobloco dos demais órgãos pélvicos envolvidos
(exenteração pélvica).5-9
Essa conduta cirúrgica, no entanto
apresenta alta morbidade aliada a substancial mortalidade.
Quando somente o reto ou cólon sigmóide em sua porção
inferior é invadido, a ressecção anterior baixa
com histerectomia total em monobloco também
designada como exenteração pélvica posterior pode ser o
suficiente. Contudo, quando ocorre à invasão
conjuntamente do trígono vesical, o procedimento padronizado é
a ressecção dos órgãos do trato urinário inferior
(bexiga e terço distal dos ureteres) e do trato genital
interno associado à ressecção anterior baixa em
monobloco (exenteração pélvica total
supra-elevadora).10 Como alternativa estratégica, com o objetivo de se evitar
cirurgias multiviscerais, a utilização da quimioterapia
neo-adjuvante tem sido recomendada em associação
a citorredução de intervalo.11-12
Embora existam poucas séries descritas na
literatura sobre o uso dessa operação no tratamento
do câncer de ovário, especificamente no Brasil não
encontramos nenhuma.
Assim sendo, o objetivo do presente estudo foi avaliar os resultados precoces e tardios
(morbidade, mortalidade e sobrevida) das pacientes com
câncer epitelial de ovário avançado submetidos a esse
tipo de operação como parte de uma cirurgia
citorredutora ótima, em uma experiência de dez anos em nosso
serviço.
MÉTODOS
Entre Janeiro de 1996 e Junho de 2006, 37 doentes com câncer epitelial de ovário avançado
(Estádios III-C e IV, FIGO) com envolvimento clínico
e/ou radiológico de estruturas pélvicas (reto, cólon
sigmóide, ureteres, bexiga) foram avaliados pelo Serviço
Cirurgia Geral e Oncocirurgia do Hospital do Servidor
Público Estadual de São Paulo, "Francisco Morato
de Oliveira". Dentre essas doentes, um total de 19
foram submetidas à ressecção anterior baixa em
monobloco (exenteração pélvica) e fizeram parte do presente
estudo. Dezessete pacientes foram submetidas
à ressecção anterior baixa do reto com histerectomia
total em monobloco (exenteração pélvica posterior) e
duas à ressecção anterior baixa do reto com
histerectomia total, ureterectomia parcial bilateral e cistectomia
total em monobloco (exenteração pélvica total
supra-elevadora). Os critérios de exclusão foram: câncer
de ovário não-epitelial, tumores bordeline,
citorredução secundária, doença recorrente, exenteração
paliativa, citorredução não-ótima, cirurgias realizadas em
outro departamento ou instituição.
Foram colhidos de maneira retrospectiva os seguintes dados de prontuário: idade, origem,
doença associada, classificação do risco cirúrgico -
ASA (American Society of Anesthesiology), estádio do
tumor, subtipo histológico e grau, sintomas
pré-operatórios, níveis séricos de CA 125, nível sérico
pré-operatório de albumina, achados radiológicos
pré-operatórios (tomografia de abdome e pelve), tipo de cirurgia,
tipo de droga usada na quimioterapia, número de
ciclos, resposta a quimioterapia, doença residual
após citorredução, hemorragia estimada
intra-operatória, tempo cirúrgico, morbidade, tempo de internação
hospitalar, mortalidade pós-operatória, número de
linfonodos dissecados, modo e tempo de recorrência, tempo
de intervalo livre de doença, sobrevida global e
sobrevida específica livre de doença.
Todas as pacientes foram estadiadas de acordo com as normas da International Federation
of Gynecology and Obstetrics System.13 A definição
de citorredução ótima adotada em nosso serviço tem
sido a descrita pelo Gynecologic Oncology Group que
considera como lesão residual menos do que 1 cm
de doença.12
Primariamente, cinco doentes foram
excluídas devido à má condição clínica pré-operatória sendo
tratadas paliativamente apenas com suporte clínico.
Conseqüentemente, das 32 restantes, dezessete já
apresentavam critérios de irressecabilidade radiológica
pré-operatória, e foram encaminhadas para
tratamento quimioterápico primário. Sendo assim, quinze
foram exploradas cirurgicamente com intuito de avaliar
sua ressecabilidade intra-operatória. Dessas quinze, em
sete foi possível a realização de uma citorredução
ótima primária (doença residual menor que 1 cm). Nos
demais (n=8), a citorredução poderia ser ótima,
contudo levaria a importante morbidade (reconstruções
complexas tanto gastrointestinais quanto urinárias,
múltiplas anastomoses gastrointestinais e
ressecções mutiladoras). Assim sendo, essas doentes (n=8)
também seguidas das demais já consideradas
irressecáveis de princípio (17) foram encaminhadas
para quimioterapia neoadjuvante.
A conduta padronizada em nosso serviço
em relação à quimioterapia neo-adjuvante tem sido: 1)
se resposta parcial, a paciente é encaminhada
a citorredução de intervalo; 2) se há ausência de
resposta ou progressão de doença, a paciente é
encaminhada a quimioterapia de segunda linha. A resposta é
avaliada por exame clínico, nível sérico de CA 125
e tomografia computadorizada (TC). O padrão de
resposta segue as determinações da
WHO. (14)
Os regimes quimioterápicos utilizados
foram todos baseados em platina associada nos casos
mais antigos à ciclofosfamida (n=5) ou mais
recentemente ao taxol (n=20). A resposta à
quimioterapia neoadjuvante foi avaliada depois do terceiro
ciclo. Dezenove doentes apresentaram resposta parcial
(índice de resposta de 76%) e conseqüentemente
foram submetidos à exploração cirúrgica. Doze
seguiram citorredução ótima, todas associadas a
exenteração (exenteração pélvica posterior = 10 e
exenteração pélvica total = 2). Dois de nove que eram
considerados irressecáveis antes da quimioterapia, se
tornaram ressecáveis após o tratamento (25 %). A
quimioterapia neoadjuvante rendeu uma citorredução ótima em
doze doentes (48 %). Mesmo assim, sete pacientes
permanecerão irressecáveis à avaliação
intra-operatória. Conseqüentemente, um total de 19 doentes
apresentou tumor ressecável, sendo sete na cirurgia primária e
doze na cirurgia de intervalo.
Ao término do tratamento todas as
pacientes foram seguidas a cada três meses (durante dois
anos), e a cada seis meses (entre dois e cinco anos). Em
cada retorno foi realizado exame físico completo, CA
125 sérico, tomografias de abdome-pelve e raio-X de
tórax. A recidiva foi somente considerada por
exames de imagem confirmados com avaliação histológica.
DESCRIÇĂO DA TÉCNICA CIRÚRGICA
A exenteração pélvica total quando
realizada seguiu os princípios técnicos já adotados em nosso
Serviço e que foram previamente
descritos. (10) Em contrapartida, os princípios técnicos da
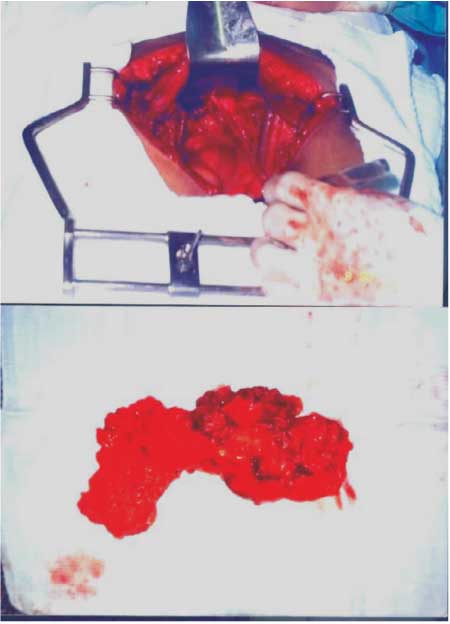
exenteração pélvica posterior (Figuras 1 e 2) seguiram aqueles
descritos por Eisenkop et al.5 Previamente à
ressecção pélvica radical, todos os doentes seguiram um
procedimento padronizado de estadiamento
anatomo-cirúrgico conforme descrito pela FIGO como: coleta de
lavado peritoneal abdominal ou pélvico (ou do
líquido ascítico), omentectomia, linfadenectomia pélvica
(ilíaco-obturatória) e retroperitoneal (para-aórtica).
As linfadenectomias tanto ilíaco-obturatória quanto
para-aórtica seguiram os princípios técnicos descritos
e adotados pelo Departamento de Oncoginecologia do Memorial Sloan Kettering Cancer (figuras 3 e 4).
A apendicectomia somente foi realizada nos casos
de adenocarcinoma mucinoso ou nos casos de comprometimento indubitável do apêndice cecal pela
neoplasia. Todas as anastomoses colorretais foram mecânicas
com o uso da técnica de duplo grampeamento. Em
duas pacientes com idade avançada que apresentavam
condição clínica de risco (ASA III), e em mais outras
duas submetidas à exenteração pélvica total, a
reconstrução utilizada foi uma colostomia terminal
(tipo Hartman). Nessas duas últimas doentes a
reconstrução urinária utilizada foi uma ureteroileostomia
cutânea a Bricker.
 |
Figuras 1 e 2 - Aspectos da pelve (foto acima) e da peça
cirúrgica (foto abaixo) - ressecção em monobloco do reto-sigmóide com útero e anexos (Exenteração Pélvica Posterior Modificada). |
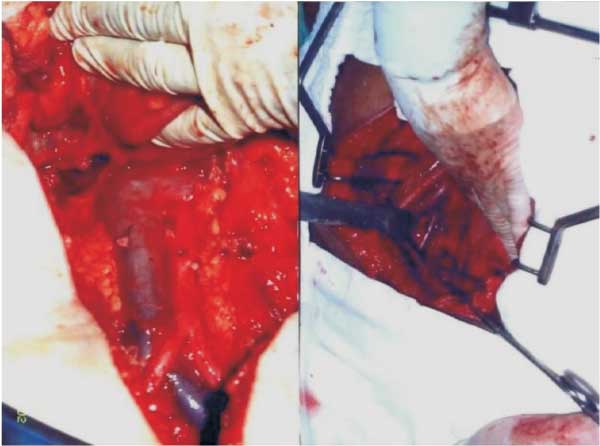 |
Figuras 3 e 4 - Linfadenectomias para-aórtica (à esquerda)
e ilíaco-obturatória (à direita). |
RESULTADOS
Os achados clínicos, histológicos e
laboratoriais estão demonstrados na Tabela 1. A mortalidade
global da presente série foi de 5% (n=1). O único óbito
dessa série foi em uma paciente submetida à
exenteração pélvica total que apresentou um grande
abscesso pélvico. Essa doente foi reoperada, e faleceu por
complicações infecciosas no trigésimo quinto dia de
pós-operatório. Por outro lado, a morbidade da
presente série foi de 26,3 % (n=5). Quinze doentes foram
submetidas à pelo menos uma outra ressecção
cirúrgica além da exenteração pélvica. (Cirurgias e
Resultados estão demonstrados na Tabela 2).
 |
 |
 |
DISCUSSĂO
A porcentagem de pacientes com câncer de ovário em estádio avançado que podem ser
submetidas à citorredução ótima varia muito na literatura.
Essa grande diferença é multifatorial e depende de
fatores como: experiência cirúrgica, local de tratamento
(centro de referência terciário) ou mesmo o entusiasmo
com a cirurgia de citorredução.
Citorredução ótima é um dos mais
importantes fatores prognósticos tanto de sobrevida livre de
doença quanto de sobrevida global nas pacientes com
câncer epitelial de ovário em estádios avançados.
(15) Para que seja atingida uma citorredução ótima nos casos
de doença pélvica extensa que comprometa
estruturas adjacentes ao trato genital feminino torna-se
necessário na maioria das pacientes uma ressecção do
reto-sigmóide ou mesmo do trato urinário inferior
(parcial ou total). A ressecção anterior baixa em monobloco
foi realizada em 16 a 58% das pacientes com câncer
de ovário nos estádios III-IV da FIGO.
(15-19)
Ao utilizar a técnica descrita como exenteração pélvica posterior modificada,
Eisenkop et al.(5) conseguiram citorredução ótima (sem
doença residual macroscópica) na pelve, em 18 de 47
(38,8%) pacientes com câncer de ovário avançado. Após
uma mediana de tempo de seguimento de 13,3 meses
em 15 (40,5%) das pacientes primariamente operadas
não foi observada recorrência pélvica. Ao estender
seu estudo inicial, Eisenkop et al.(20) avaliaram 163
pacientes com câncer de ovário avançado e
realizaram exenteração pélvica posterior modificada
com anastomose retal baixa em 85 pacientes (52, 1%)
com sucesso. Em 139 desses 163 pacientes (85,35 %)
todo implante tumoral visível macroscopicamente fora
removido. Benedetti-Panici et al.(21) ao descreverem
a abordagem retroperitoneal para o tratamento do
câncer de ovário, realizada em 66 de 147 pacientes
com neoplasia avançada (45%), verificaram que
a ressecção colorretal foi necessária em 14 de 66
pacientes (21%).
Com essa abordagem estes autores puderam atingir uma citorredução ótima (menos de 5 mm
de maior implante tumoral residual) em 60
pacientes (91%). Tais estudos demonstraram o importante
papel das ressecções multiviscerais
pélvicas (exenteração) na obtenção de uma citorredução
ótima nas pacientes com câncer de ovário avançado
com o objetivo de aumentar sua sobrevida. No
presente estudo também pôde se observar que a
exenteração pélvica proporcionou citorredução ótima em todas
as doentes, sendo que na maioria não se observou
doença macroscópica ao término da operação (78%
cirurgia sem resíduo macroscópico). No entanto, em
nosso ponto de vista, essa extensa operação
somente permanece justificada quando todo o volume
tumoral tanto da pelve quanto do abdome superior pode
ser totalmente citorreduzido a menos do que 1 cm de
doença residual. Mesmo assim, essa conduta pode
levar a considerável morbidade e significante
mortalidade. A morbidade da presente série foi similar à
descrita por outros autores.5-8 Realizamos um maior
número de reintervenções (23,52%), quatro doentes
foram reoperadas na mesma internação. A despeito
da pequena amostra, três desses casos (75%) foram
do grupo submetido à citorredução primária. Esse
fato foi mais comumente encontrado nas pacientes
submetidas a múltiplas ressecções de órgãos além
da exenteração, incluindo cinco hemicolectomias,
três cistectomias parciais e uma hepatectomia parcial
entre outros procedimentos maiores.
Resultados similares foram observados por Mohamed et
al.11 sinalizando que a citorredução de
intervalo após quimioterapia neo-adjuvante, deva ser
realizada quando existe a possibilidade de um
procedimento alargado com múltiplas ressecções
e anastomoses para se atingir uma citorredução
ótima. As complicações maiores dessa série como
abscessos intra-cavitários devido às fístulas tanto de
anastomose colorretal quanto de intestino delgado, também têm
sido descritas por outros autores quando se trata
de citorredução ótima com ressecções
multiviscerais.6, 7
Um escape da anastomose colorretal baixa pode acontecer mesmo com a confecção de
uma ostomia protetora. Na presente série, a
porcentagem de fístula na anastomose colorretal baixa foi de 6
% similar ao encontrado por outros autores que variou
de 0 % a 14 %.21-27
Mesmo assim, essa fistula ocorreu em um caso extremo, onde a doente foi submetida a uma
ressecção de múltiplos órgãos (ressecção do diafragma
e esplenectomia) e apresentava o mais baixo valor
de albumina sérica dessa série, bem como o
maior sangramento intra-operatório (4500 ml). Em séries
reportadas previamente, é fato conhecido que tanto
níveis baixos de albumina quanto grande número de
transfusões estão associados a maior risco de fístula
de anastomose. (6) A despeito da drenagem percutânea
de abscesso ser uma conduta de primeira escolha para
o tratamento dos abscessos pélvicos ou abdominais
acessíveis, nos três casos da presente casuística sua
resolução foi por laparotomia. Contudo, esses casos
foram dos mais antigos da série, quando a
drenagem percutânea não era disponível e nem padronizada
em nosso serviço. Paralelamente, alguns autores crêem
que mesmo com uma drenagem percutânea adequada,
uma reintervenção pode muitas vezes não ser evitada.
(6, 7) Temos utilizado ostomia de proteção seletivamente
para pacientes irradiados, quando a anastomose não
fica segura ou é muito baixa (colo-anal). Assim sendo,
nosso número de ostomias de proteção (50 %) foi
próximo ao descrito por outros autores.
(5, 8)
Em nosso meio, poucas séries específicas
de ressecção anterior baixa em monobloco
(exenteração pélvica) têm sido descritas para o tratamento
de neoplasias pélvicas avançadas.
Particularmente para o câncer de ovário
avançado, não encontramos estudo similar no que tange
seu tratamento com intenção curativa por meio
de ressecções multiviscerais pélvicas (exenteração)
como parte da estratégia de "Optimal Debulking".
Na presente série, o índice de citorredução
ótima foi 56,66% similar aos resultados mais
recentemente publicados por outros autores que têm variado de 50
a 75%.5-28 A despeito da alta morbidade, a
exenteração como parte da cirurgia de citorredução tem
apresentado diminuição da mortalidade pós-operatória,
mormente nas últimas séries que tem variado entre 0 % e
6 %.5-30 No presente estudo a mortalidade foi similar
inclusive com série descrita previamente pelo
mesmo grupo para o tratamento do câncer de reto T4 que
foi de 6 %.(10) Mesmo considerando cirurgias
abdominais extensas associadas à exenteração como parte
da citorredução na maioria de nossos casos (90%)
similar ao descrito por Eisenhauer et al.
(31), a presente mortalidade pode ser considerada dentro do esperado na
literatura.
Embora nenhum teste estatístico
específico tenha sido feito no presente estudo, a mediana
de sobrevida global das pacientes submetidas a
ressecção anterior baixa em monobloco foi maior (42 meses X
13 meses) do que a daquelas que não a
seguiram (quimioterapia exclusiva, citorredução subótima,
tratamento paliativo). E paralelamente, a sobrevida
global em três anos foi maior de 77% contra 0%. Por
outro lado, a sobrevida livre de doença no mesmo grupo
foi de 44%, ou seja, houve uma alta recorrência
principalmente no peritônio ou na pelve. Sendo que não
houve sobreviventes em cinco anos, mesmo para aquelas
submetidas à ressecção anterior baixa em monobloco
com citorredução ótima.
Nossos resultados são semelhantes aos
observados por Buttarelli et al. (6) que observaram uma
mediana de sobrevida de 36,6 meses. Mais
recentemente, Park et al. (30) também observaram 30 meses
de sobrevida mediana para doentes submetidas a esse
tipo de cirurgia. Esses últimos observaram uma
sobrevida em três anos de 82, 03%, para o grupo submetido
a ressecção anterior baixa em monobloco
com citorredução ótima contra 66, 63 % nas doentes
não submetidas a essa técnica (p=0.04). Assim sendo,
esses achados suportam a realização de uma
cirurgia pélvica extensa com ressecção multivisceral como
parte do tratamento do câncer de ovário avançado,
principalmente quando uma citorredução ótima pode
ser exeqüível.
Apesar de ser conduta de exceção, além
de proporcionar um prolongamento da sobrevida pode
também melhorar os sintomas importantes do câncer
de ovário avançado. A obstipação, o tenesmo ou a
dor pélvica podem ser temporariamente controlados
com essa técnica podendo assim acarretar uma melhor
qualidade de vida para esses
doentes.5-8 Embora não tenha sido elaborado um questionário sobre qualidade
de vida no presente estudo, pode-se observar um
melhor controle temporário dos sintomas na maioria das
pacientes operadas. Similar a Butarelli et al.
(6), a preservação da continência fecal foi possível em todas
doentes submetidas à anastomose colorretal baixa,
melhorando assim a sua qualidade de vida. Todas as
doentes retornaram a suas atividades diárias. Os sintomas
pré-operatórios foram bem controlados em 88 % das
doentes, durante uma mediana de tempo livre dos
sintomas de 20 meses.
CONCLUSĂO
Em suma, a ressecção anterior baixa
em monobloco como parte da cirurgia citorredutora para
o tratamento do câncer epitelial do ovário avançado
não deve ser um obstáculo se a citorredução ótima
é factível. Apresenta alta morbidade, porém baixa
mortalidade. Pode conferir um adequado controle da
doença em longo prazo, à custa de uma alta
recorrência tardia. Paralelamente, os sintomas pré-operatórios
também podem ser temporariamente controlados.
ABSTRACT: Introduction - The cornerstone of ovarian cancer treatment has been the association of debulking surgery with platinum based chemotherapy. When this neoplasm invades adjacent pelvic organs, in order to attain an optimal debulking should be performed an en bloc multivisceral pelvic resection. Aim - The objectives of this study were to assess the safety, efficacy and impact on survival of low anterior en bloc resection for primary advanced epithelial ovarian cancer. Methods - Complete follow-up data were available on 19 patients who underwent this surgical procedure for advanced ovarian cancer between January 1996 and June 2006. These subjects presented a median age of 58 years (24-77). All patients underwent optimal cytoreduction (less than 1cm of residual disease). Results - The postoperative mortality was 5 % (n=1) while overall major morbidity was 26,3 % (n=5).The overall three-year survival rate was 77 % while median of survival time was 42 months. Conclusions - Low anterior en bloc resection, when it is necessary must not be obstacle to obtain an optimal surgery. In despite its high morbidity presents acceptable mortality. Long-term disease control may be attained with this approach.
Key words: Pelvic Exenteration, Ovarian Cancer, Morbidity, Mortality, Treatment Outcome.
Referências
1. Karlan BY, Markman MA, Eifel PJ. Gynecologic
Cancers: Ovarian cancer, Peritoneal carcinoma, and Fallopian Tube
carcinoma. In: DeVita VT, Helman S, Rosenberg SA eds.
Cancer: Principles & Practice of Oncology, 7 th Edition,
Philadelphia: Lippincot & Wilkins; 2005. pp. 1240-65.
2. Hensley Ml, Alektiar KM, Chi DS. Ovarian and
fallopian-tube cancer. In: Barakat RR, Bevers MW, Gershenson
DM, Hoskins WJ eds. MD Anderson Cancer Center &
Memorial Sloan-Kettering Cancer Center Handbook of
Gynecologic Oncology, 1 Th Edition, London: Martin Dunitz; 2000.
pp. 243-263.
3. Hoskins WJ, Lawton FG. Primary Cytoreductive Surgery
for Advanced-Stage Disease. In: Gershenson DM, McGuire
WP editors. Ovarian Cancer Controversies in Management, 1
th Edition, New York: Chuchill Livingstone; 1998. pp. 65-84.
4. Slomovitz BM, Soliman PT, Wolf JK. Gynecologic
Cancers. In: Feig BW, Berger DH, Fuhrman GM editors. The
M.D. Anderson Surgical Oncology Handbook, 4 th
Edition, Philadelphia: Lippincott Williams & Wilkins; 2006. pp.
520-563.
5. Eisenkop SM, Nalick RH, Teng NNH. Modified
Posterior Exenteration for Ovarian Cancer. Obstetrics &
Gynecology 1991; 78 (5): 879-85.
6. Butarelli M, Houvenaghel G, Leliévre L, Jacquemier
J, Guimarand J, Delpero JR. Pelvic posterior exenteration
with immediated colo-rectal anastomosis: Is it justified and
feasible in advanced stage ovarian carcinoma? Ann Chir 2006;
131: 431-6.
7. Mourton SM, Temple LK, Abu-Rustum NR, Gemignani
ML, Sonoda Y, Bochner BH, Brakat RR, Chi DS. Morbity
of retosigmoidectomy resection and primary anastomosis
in patients undergoing primary cytoreductive surgery
for advanced epithelial ovarian cancer. Gynecol Oncol 2005;
99: 608-14.
8. Spirtos NM, Eisenkop SM, Schlaerth JB, Ballon SC.
Second-look laparotomy after modified posterior exenteration:
Patterns of persistence and recurrence in patients with stage III
and stage IV ovarian cancer. Am J Obstet Gynecol 2000; 182
(6): 1321-27.
9. Tamussino KF, Lim PC, Webb MJ, Lee RA, Lesnick
TG. Gastrointestinal Surgery in Patients with Ovarian
Cancer. Gynecol Oncol 2001; 80: 79-84.
10. Costa SRP, Antunes RCP, Paula RP, Pedroso MA, Farah
JFM, Lupinacci RA. A Exenteração Pélvica para o Tratamento
do Câncer de Reto Estádio T4: Experiência em 15 casos
operados. Arq Gastroenterol 2007; 43 (4): no prelo.
11. Vergote I, Wever I, Tjalma W, Van Gramberen M, Decloedt
J, Vam Dam P. Interval Debulking Surgery: An Alternative
for Primary Surgical Debulking? Semin Surg Oncol 2000; 19:
49-53.
12. Hegazy MAF, Hegazi RAF, Elsshafei MA, Setit AE,
Elshamy MR, Eltatoongy M, Halim AAF. Neoadjuvant
chemotherapy versus primary surgery in advanced ovarian carcinoma.
WJSO 2005; 3: 57.
13. Staging announcement: FIGO Cancer Committee.
Gynecol Oncol 1986; 25: 383-5.
14. Gallo A, Frigerio L. Neoadjuvant chemotherapy and
surgical considerations in ovarian cancer. Curr Opin Obstet
Gynecol 2003; 1: 25-31.
15. Bristow RE, Tomacruz RS, Armostrong DK, Trimble
EL, Montz FJ. Survival effect of maximal cytoreductive
surgery for advanced ovarian carcinoma during the platinum era:
a meta-analysis. J Clin Oncol 2002; 20: 1248-59.
16. Hacker NF, Bereck JS, Lagasse LD, Nieberg RK,
Elashoff RM. Primary cytoreductive surgery for epithelial
ovarian cancer. Obstet Gynecol 1983; 61: 413-20.
17. Guidozzi F, Ball JH. Extensive primary cytoreductive
surgery for advanced epithelial ovarian cancer. Gynecol Oncol
1994; 53: 326-30.
18. Munkarah AR, Hallum AV 3rd, Morris M, Burke
TW, Levenbeck C, Atkinson EN et al. Prognostic significance
of residual disease in patients with stage IV epithelial
ovarian cancer. Gynecol Oncol 1997; 64: 31-7.
19. Lichtenegger W, Sehouli J, Buchmann E, Karajenev
C, Weideman H. Operative results after primary and
secondary debulking operations in advanced ovarian cancer. J Obstet
Gynaecol Res 1998; 24 447-51.
20. Eisenkop SM, Friedmann RL, Wang H.
Complete cytoreductive surgery is feasible and maximizes survival
in patients with advanced epithelial ovarian cancer: a
prospective study. Gynecol Oncol 1998; 69: 103-8.
21. Benedetti-Panici, Maneschi F, Scambia G, Cutillo G, Greggi
S, Mancuso S. The pelvic retroperitoneal approach in
the treatment of advanced ovarian carcinoma. Obstet
Gynecol 1996; 87: 103-8.
22. Obermair A, Hagenauer S, Tamandl D. Safety and efficacy
of low anterior em bloc resection as part of cytoreductive
surgery for patients with ovarian cancer. Gynecol Oncol 2001;
83: 115-20.
23. De la Cuesta RS, Goodman A, Halverson SS, Fuller Jr AF.
En bloc pelvic peritoneal resection of the intraperitoneal
pelvic viscera in patients with advanced epithelial ovarian
cancer. Cancer J Sci Am 1996; 2: 152.
24. Bristow RE, del Carmen MG, Kaufman HS, Montz FJ.
Radical oophorectomy with primary stapled
colorectal anastomosis for resection of locally advanced epithelial
ovarian cancer. J Am Coll Surg 2003; 197: 565-774.
25. Sonnendecker EW, Beale PG. Rectosigmoid resection
without colostomy during primary cytoreductive for ovarian
carcinoma. Int Surg 1989; 74: 10-2.
26. Clayton RD, Obermair A, Hammond IG, Leung
YC, McCartney AJ. The Western Australian experience of the
use of en bloc resection of ovarian cancer with
concomitant rectosigmoid colectomy. Gynecol Oncol 2002; 84: 53-7.
27. Soper JT, Couchman G, Berchuck A, Clarke-Pearson D.
The role of partial sigmoid resection for debulking epithelial
ovarian carcinoma. Gynecol Oncol 1991; 41: 239-44.
28. Scarabelli C, Gallo A, Francheschi S. Primary
cytoreductive surgery with rectosigmoid colon resection for
patients with advanced epithelial ovarian cancer. Cancer 2000;
88: 389-97.
29. Hertel H, Diebolder H, Herrmann J, Kohler C, Kune-Heid
R, Possover M et al. Is the Decision for Colorectal
Resection Justified by Histopathologic Findings: A Prospective
Study of 100 patients with Advanced Ovarian Cancer. Gynecol
Oncol 2001; 83 (3): 481-4.
30. Park JY, Seo SS, Kang S, Lee KB, Lim SY, Choi HS, Park
SY. The benefits of low anterior en bloc resection as part
of cytoreductive surgery for advanced primary and
recurrent epithelial ovarian cancer patients outweigh morbidity
concerns. Gynecol Oncol 2006; 103 (3): 977-84.
31. Eisenhauer EL, Abu-Rustum NR, Sonoda Y, Levine
DA, Poynor EA, Aghajanian C et al. The addition of
extensive upper abdominal surgery to achieve optimal
cytoreduction improves survival in patients with stages III-C-IV
epithelial ovarian cancer. Gynecol Oncol 2006 103 (3): 1083-90.
Endereço para correspondência:
Sergio Renato Pais Costa
Instituto de Oncologia São Paulo
Avenida Pacaembu, 1400,
CEP: 01234-200
Tel.: 11- 3666-2299
E-mail: sergiorenatopais@ig.com.br
Recebido em 08/01/2008
Aceito para publicação em 04/03/2008
Trabalho realizado no Serviço de Cirurgia Geral e Oncocirurgia do Hospital do Servidor Público Estadual de São Paulo - "Francisco Morato de Oliveira".