
ARTIGOS ORIGINAIS
PESQUISA DE LINFONODO-SENTINELA EM PACIENTES COM ADENOCARCINOMA DE CÓLON
Sentinel Lymphonode Research in Patients with Colon Cancer
AntÔnio HilÁrio Alves Freitas1, Tarcizo Afonso Nunes2, Alberto Julius Alves Wainstein3, Adelanir AntÔnio Barroso4, Omar de Paula Ricardo-Filho5, Marco AntÔnio Dias5, Marco AntÔnio Dias-Filho5, Waldemar Nascimento BrandÃo Penna6
1Titular da Sociedade Brasileira de Coloproctologia, 2Professor UFMG, 3Pesquisador Biocâncer, 4Médico Nuclear, 5Patologista, 6Médico Residente.
RESUMO: O câncer colorretal é responsável por cerca de 8.000 óbitos/ano no Brasil. Acredita-se que haja subestadiamento pós-operatório. O objetivo deste trabalho é pesquisar sobre linfonodo-sentinela em pacientes com adenocarcinoma de cólon. A amostra foi composta de 18 pacientes, todos com diagnóstico de adenocarcinoma de cólon, submetidos à laparotomia com injeção dos marcadores de linfonodos na subserosa peritumoral. Resultados: a identificação intra-operatória de linfonodo-sentinela com os marcadores ocorreu em 16 (88,8%) pacientes. O azul patente identificou linfonodos-sentinela em 72,2% e o fitato marcado com tecnécio em 88,8%. Obtiveram-se linfocintilografias do espécime cirúrgico removido em 15 pacientes. A sensibilidade global do método foi de 66,7% e o falso negativo de 33,3%. Depois do exame histológico com multissecção e imunoistoquímica de 11 pacientes, foi diagnosticada metástase em uma (9%) ocorrência, sendo considerada ultra-estadiamento. Conclusões: pode-se afirmar que o procedimento é viável; o radiofármaco é mais eficaz; a linfocintilografia da peça cirúrgica é capaz de certificar a presença de captação de radiofármaco pelo linfonodo; a incidência de metástases linfonodais é, proporcionalmente, a mesma nos linfonodos-sentinela e não-sentinela; as técnicas de multissecção e imunoistoquímica contribuem para melhorar a acuidade diagnóstica de metástase linfonodal.
Descritores: Linfonodo-sentinela, Câncer, Cólon, Metástases.
INTRODUÇĂO
A incidência de câncer colorretal no Brasil
é de aproximadamente 25.000 casos por ano
1. O tratamento de escolha para tumores de cólon é a
remoção em bloco da neoplasia e de todos os tecidos
envolvidos na drenagem linfática, que é a principal via de
disseminação desses tumores
2. Os estadiamentos clássicos propostos têm como principal objetivo
diagnosticar metástase nos linfonodos. Quando presente, o
paciente é encaminhado para quimioterapia adjuvante,
que aumenta o tempo livre de doença e a sobrevida
3.
Sabe-se que um quarto dos pacientes operados por adenocarcinoma de cólon e sem linfonodos
comprometidos à histologia de rotina, portanto, sem indicação
de terapia adjuvante, evolui para óbito em até cinco anos
por recorrência local do tumor ou metástase à distância
4, 5, 6.
O linfonodo-sentinela é considerado o
primeiro a receber drenagem linfática do tumor e, desta forma,
o mais provável de conter metástases
7. Nele, podem-se empregar meios diagnósticos mais eficazes, como
exame histológico com multissecção e
imunoistoquímica, inviáveis e de alto custo para serem realizadas em
todos os linfonodos dissecados 8.
Diante desses fatos, este trabalho se propõe
a avaliar a pesquisa de linfonodo-sentinela nos
tumores do intestino grosso por meio de corante e
radiofármaco no perioperatório; e utilizar além da histologia de
rotina com hematoxilina-eosina, a multissecção de
linfonodos e a imunoistoquímica com citoqueratinas, com o
objetivo de melhorar o estadiamento final dos pacientes
e, assim, contribuir para aumentar o índice de cura
dessa afecção.
PACIENTES E MÉTODOS
Trata-se de estudo prospectivo, descritivo e analítico, sobre linfonodo-sentinela em indivíduos
com adenocarcinoma de cólon, operados
exclusivamente pelo autor desta pesquisa, no período de abril de 2005
a fevereiro de 2007, no Hospital Alberto Cavalcanti,
que pertence à rede pública estadual de saúde da
Fundação Hospitalar do Estado de Minas Gerais
(FHEMIG), Belo Horizonte, Brasil.
Aprovado pelo Comitê de Ética em
Pesquisa (CEP) da Fundação Hospitalar do Estado de
Minas Gerais (FHEMIG), parecer n° 290; e pelo Comitê
de Ética em Pesquisa (COEP) da Universidade
Federal de Minas Gerais (UFMG) parecer n° 168.
Todos os pacientes tiveram avaliação no
pré-operatório, e diagnóstico histológico de
adenocarcinoma de cólon com proposta de cirurgia curativa.
Os critérios de inclusão foram: pacientes
com adenocarcinoma de cólon e adesão ao termo de
consentimento. Os de exclusão foram: evidência de
invasão de órgão adjacente ou metástase distante;
tumor de origem não identificada nos últimos cinco anos;
cirurgia prévia na região que possa alterar a
drenagem linfática local; gravidez; recusa do paciente.
A marcação dos linfonodos foi realizada
da seguinte forma: a) injeção intra-operatória com
seringa na subserosa em quatro pontos cardeais
adjacentes ao tumor de corante azul patente: volume de 1 ml,
concentração a 1%, fabricado pela Citopharma Ltda
(Belo Horizonte - M.G.) (figura 1). b) injeção de
fármaco radioativo (Fitato 99mTecnécio) na dose de 1,2 mci
em volume de 0,8 ml, liofilizado, estéril, apirógeno,
produzido e distribuído pelo Instituto de Pesquisa de
Energia Nuclear (IPEN) (São Paulo - S.P.), do mesmo
modo descrito anteriormente para o corante.
 |
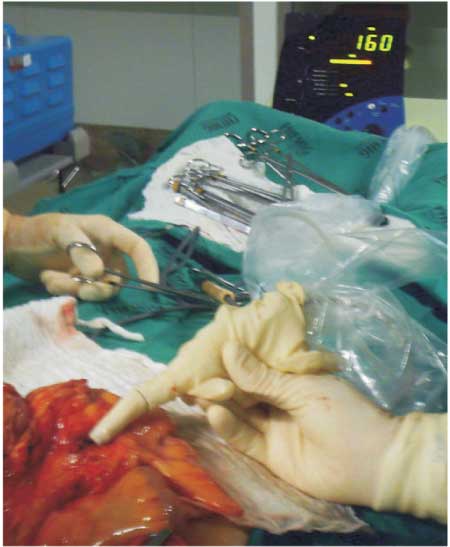
Figuras 1 - Fotografia digital da injeção do marcador de
linfonodos peri-tumoral. |
 |
Figuras 2 - Fotografia digital da identificação peroperatória dos linfonodos captantes por meio do gama probe. |
 |
Figuras 3 - Linfocintilografia da peça cirúrgica com imagem
da área de injeção do radiofármaco e migração do marcador para os linfonodos-sentinela. |
RESULTADOS
Identificação dos linfonodos pelo azul
patente e radiofármaco
Nas peças cirúrgicas dos 18
participantes, foram isolados 238 linfonodos, média de
13,2 (DP=5,1) por paciente. Foram identificados
46 linfonodos-sentinela no intra-operatório por
meio do corante e radiofármaco em 16 (88,8%),
com média de 2,8 (DP=0,9) por paciente. O azul
patente identificou linfonodo-sentinela em 13 (72,2%) indivíduos e o radiofármaco em
16 (88,8%) casos. Em dois pacientes não
foram identificados linfonodos-sentinela por nenhum
dos marcadores.
Não foram identificados linfonodos
corados ou captantes fora da área de ressecção, e por isso
a extensão da operação, que foi oncológica e
radical, não teve de ser ampliada. Dois apresentaram
urina azul após injeção do corante, que desapareceu
em aproximadamente quatro horas, não acarretando
qualquer conseqüência posterior. Não houve
qualquer outro evento adverso decorrente da pesquisa
de linfonodo-sentinela (tabela 1).
 |
Linfocintilografia
Foram obtidas imagens das peças
cirúrgicas de 15 pacientes, o que não foi possível nos outros
três por problemas logísticos. Nos dois casos em que
os linfonodos-sentinela não foram identificados no
intra-operatório, também não foram detectadas imagens
de linfonodos por cintilografia.
Treze pacientes tiveram linfonodos-sentinela identificados no intra-operatório e também foram
realizadas imagens na gama-câmara. Em 12 (92,3%)
destes apareceram linfonodos na imagem e em apenas um caso (7,7%) a linfocintilografia não mostrou
imagem de linfonodo.
Marcadores de linfonodos e histologia
Entre os 46 linfonodos-sentinela identificados pelos marcadores, o exame histológico de rotina
com hematoxilina-eosina diagnosticou metástases em
seis (13,0%), e nos outros 40 (87,0%) não foram
encontrados sinais de metástases. Dos 192 linfonodos
não-sentinela, 24 (12,5%) continham metástases e 168
(87,5%) estavam livres de metástases (tabela 2).
 |
 |
 |
Estadiamento dos pacientes
O exame histológico de rotina não
diagnosticou metástase em 11 (61,1%) dos 18
pacientes, portanto, eles foram considerados estádio N0.
Nos outros sete (38,9%), foram diagnosticadas metástases, sendo classificados no estádio N1
ou N2. Dessa forma, o estadiamento (TNM) inicial
da amostra foi:
· Estádio I = 02 pacientes (11,1%);
· Estádio II = 09 pacientes (50,0%);
· Estádio III = 07 pacientes (38,9%).
No grupo dos 11 pacientes sem metástases
pela histologia de rotina (estádios I ou II), os exames
por multissecção e imunoistoquímica
diagnosticaram metástase em apenas um (9,0%). O
estadiamento (TNM) final, então, foi:
· Estádio I = 02 pacientes (11,1%);
· Estádio II = 08 pacientes (44,45%);
· Estádio III = 08 pacientes (44,45%).
DISCUSSÃO
Identificação dos linfonodos
O mapeamento linfático do câncer de cólon
é realizado pela maioria dos autores com
injeção subserosa dos marcadores de linfonodos (corantes
e/ou fármacos radioativos) no intra-operatório,
método utilizado no presente estudo.
Neste estudo, empregou-se a técnica
combinada (corante e radiofármaco), pois não há
consenso de qual seria o melhor marcador
10, 11, 12. Apesar de mais trabalhosa, ainda foi acrescida a
linfocintilografia, na busca por melhores resultados. O índice de
sucesso na identificação de linfonodos-sentinela
em adenocarcinomas de cólon foi de 88,8%. Isto mostra
a viabilidade técnica, já que mesmo no projeto piloto
com os quatro primeiros casos não houve dificuldade com
o método empregado, fato verificado por Paramo
et al. 13, que calcularam a curva de aprendizado, sendo
necessários cinco pacientes.
Basílio e Fonseca 14, no Rio de Janeiro,
utilizaram o corante e identificaram linfonodos-sentinela
em todos os 31 pacientes estudados.
Saha et al. 15, equipe com mais
experiência mundial nesse método, afirmaram que a utilização
da técnica combinada, apesar de mais trabalhosa,
pode aumentar a detecção de linfonodos-sentinela em
pacientes com tumores de cólon. Patten et al.
16 discordam, uma vez que em sua avaliação a
sensibilidade permaneceu inalterada quando se utilizou corante
associado ao fármaco radioativo.
Doekhie et al. 17 revisaram 25 estudos,
sendo que destes, 19 utilizaram o corante azul
como marcador, quatro técnicas combinadas de azul
mais radiofármaco, e em apenas dois o fármaco
radioativo isoladamente, com 89% de sucesso na
identificação dos linfonodos-sentinela. Em recentes revisões de
trabalhos relevantes, levando-se em consideração
diferentes técnicas, a identificação de
linfonodo-sentinela variou de 71 a 100% 18,
19.
Marcadores
Neste estudo, o desempenho do fitato radioativo foi melhor que o do corante azul patente para
identificação de linfonodos-sentinela. Todos aqueles
com linfonodos metastáticos e que tiveram linfonodos
corados de azul, foram também captantes de
radiofármaco, ou seja, o fármaco radioativo agregou valor na
identificação de linfonodo-sentinela.
Hipótese que poderia explicar tal fato seria
a desvantagem da farmacocinética do corante azul
com rápida passagem pelo linfonodo e metabolização
instantânea pelo sistema imunológico. Falhas técnicas
também podem ocorrer na injeção dos marcadores
20, 21, 22.
Linfocintilografia
Foram obtidas imagens das peças
cirúrgicas levadas à gama-câmara de 15 pacientes envolvidos
no trabalho, que serviram para certificação da
captação pelos linfonodos do radiofármaco injetado no
intra-operatório. Nos dois (12,2%) pacientes em que
os linfonodos-sentinela não foram identificados pelos
métodos intra-operatórios, também não foi detectada
imagem de linfonodo no mesocólon.
Poucos trabalhos foram publicados sobre este tema, provavelmente devido ao alto custo, que seria
o fator limitante principal, já que o valor de
cada linfocintilografia é de aproximadamente 600 dólares
ou 1.200 reais. Merrie et al. 21 fizeram
linfocintilografia objetivando localizar os linfonodos radiocaptantes
no mesocólon do espécime cirúrgico, e obtiveram
resultados favoráveis.
Captação dos marcadores e histologia
O número de linfonodos obtidos do
espécime cirúrgico é de grande importância para
estadiamento, tratamento e prognóstico dos pacientes operados
de adenocarcinoma de cólon. Nos 18 casos estudados,
foi encontrada média de 13,2 linfonodos por paciente,
que de acordo com a literatura é suficiente
para estadiamento confiável 23, 24,
25. Não existiu
correlação significativa (p=0,88) entre linfonodo-sentinela e a
presença de metástase.
Falso-negativo e sensibilidade
O alto índice de falso-negativo (33,3%)
é significativo, mas não interfere na terapêutica,
já que a linfadenectomia cirúrgica radical é
mantida nas operações de adenocarcinomas de cólon,
independentemente da presença ou ausência
de metástases nos linfonodos regionais. De acordo
com os trabalhos de revisão, a taxa global média de
falso-negativo é de 33%, variando de 0 a 63%.
Quando observados somente os trabalhos que
utilizaram o método combinado (corante e
radiofármaco), como nesta avaliação, a taxa média foi de
28%, variando de 0 a 50% 19, 27, 29.
De acordo com o estudo de validade deste trabalho, a sensibilidade foi 66,7%, enquanto na
literatura varia de 40 a 100% 17, 26,
28.
Há um consenso que quanto mais
avançado for o tumor, mais alto deverá ser o índice de
falso-negativo e menor a sensibilidade. Como este
trabalho foi desenvolvido em hospital público e os
pacientes geralmente têm dificuldade para realização
de propedêutica, esta seria uma provável causa para
justificar os valores encontrados. Ressalta-se que
38,9% dos pacientes já se encontravam no estádio
III (linfonodos com metástases) depois da histologia
de rotina com hematoxilina-eosina.
Estadiamento
De acordo com o padrão de exame
histológico de rotina, o tecido é examinado por meio de
secção simples do linfonodo. Estima-se que o material
levado a exame microscópico corado pela
hematoxilina-eosina corresponda a menos de 1% do tecido do
linfonodo, podendo ser motivo potencial de erro
30, 31.
Neste estudo, em um (9%) paciente foi encontrada micrometástase em linfonodo-sentinela
depois da realização de exame histológico complementar,
utilizando técnicas de multissecção dos linfonodos e
de imunoistoquímica. Segundo Cohen et
al. 32, poderia representar um caso de provável subestadiamento,
cujo perfil se beneficiaria da pesquisa de
linfonodo-sentinela por ter o diagnóstico de sua doença
ainda micrometastática, quando as chances de
proporcionar a cura com uma quimioterapia adjuvante seriam
maiores por atacar o tumor em fase inicial.
O ultra-estadiamento por meio de
multissecção e imunoistoquímica foi 4-47% na revisão de Tuech
et al. 26; de 37,5% segundo Codignola
et al. 33; e variou de 0-50% na revisão de Doekhie
et al. 17.
O'Brien et al. 34 objetivaram melhorar
o estadiamento dos linfonodos utilizando
método imunoistoquímico para diagnóstico de
micrometástases (depósitos isolados ou grupos de células tumorais,
de acordo com Huvus et al. 35). Verificou-se que em
cinco estudos os resultados foram favoráveis, e em
nove não foram observados efeitos na evolução dos
pacientes 26. Wong et al.
36 verificaram que nos linfonodos-sentinela há mais presença de metástases ocultas
que nos não-sentinela, mas como utilizaram
metodologias diferentes para exame dos linfonodos, tiveram a
validade de seus achados muito questionada.
Portanto, são necessários mais
trabalhos confiáveis e com grandes amostras para avaliação
do real papel das micrometástases na evolução,
na sobrevida e também a aplicabilidade prática, para
que possa ser respondido se os pacientes operados
de adenocarcinoma de cólon deveriam ou não
receber terapia adjuvante nessas situações especiais
37, 38.
CONCLUSÕES
Diante do resultado da pesquisa de linfonodo-sentinela por meio de corante e radiofármaco
no perioperatório de pacientes com adenocarcinoma
de cólon, pode-se afirmar que: o procedimento é
viável, seguro e com índice de sucesso elevado; a
associação dos marcadores é benéfica, porém o radiofármaco
é mais eficaz; a linfocintilografia da peça cirúrgica é
capaz de certificar a presença de captação
de radiofármaco pelo linfonodo; a incidência de
metástases linfonodais é, proporcionalmente, a mesma
nos linfonodos-sentinela e não-sentinela, e
falso-negativo de 33%, portanto a linfadenectomia radical deve
ser usada em todos os casos; as técnicas de
multissecção e imunoistoquímica alteraram o estadiamento em
um dos pacientes do estudo, contribuindo para melhorar
a acuidade diagnóstica de metástase linfonodal.
ABSTRACT: The colorectal cancer is responsible for 8.000 deaths a year in Brazil. It is believed that there is post operative sub staged. The objective of this study is to research on the sentinel lymph node in patients with colon cancer. The sample was composed by 18 patients, all of them with diagnose of cancer, undertaken to laparotomy with injection of the markers of lymph nodes in the subserosa peritumoral. Results: intraoperative identification sentinel lymph nodes with the markers occurred in 16 (88,8%) patients. The patent blue dye identified sentinel lymph nodes in 13 (72,2%) and the radioisotopic in 16 (88,8%). Lymphoscintigraphy of surgical specimen were obtained from 15 patients. The global sensitivity of this method was of 66,7% and the false-negative of 33,3%. After the histological examination with multilevel section and immunohistochemical in 11 patients, one (9%) case of micrometastase was diagnosed being considered ultrastaging. Conclusions: It can be said that the procedure is viable; the radioisotope is more effective; the lymphoscintigraphy of the surgical specimen is capable of certifying the presence of absorption of the radioisotope by the lymph node; the incidence of lymph node metastases is, proportionally, the same as the one of the sentinel and non sentinel nodes; the techniques of the multilevel section and immunohistochemical contribute to improve the activity of the lymph node metastases diagnose.
Key words: Sentinel lymph node, Cancer, Colon, Metastases.
Referências
1. Instituto Nacional do Câncer (INCA), 2006. Disponível
em: http://www.inca.gov.br.
2. Gordon PH, Nivatvongs S. Principles and practice of
surgery for the colon, rectum, and anus, 2th ed. St Louis,
Missouri: Quality medical Publishing, Inc., 1999.
3. Wolmark N, Rockette H, Mamounas EP. The relative efficacy
of 5-FU + leucovorin (FU-LV), 5-FU + levamisole (FU-Lev) and
5-FU + leucovorin + levamisole (FU-LV-Lev) in patients
with Dukes B and C carcinoma of the colon: first report of NSABP
C-04 [abstract 460]. Proc Am Soc Clin Oncol, 1996; 15:205.
4. Bilchick AJ, Nora DT. Lymphatic mapping of
nodal micrometastasis in colon câncer: putting the cart before
the horse? Ann Surg Oncol, 2002; 9:529-531.
5. Bertoglio S, Sandrucci S, Percivale P, Goss M, Gipponi
M, Moresco L, Mussa B, Mussa A. Prognostic value of
sentinel lymph node biopsy in the pathologic staging of
colorectal cancer patients. J Surg Oncol, 2004; 85:166-170.
6. Saha S, Seghal R, Patel M, Doan K, Dan A, Bilchick A,
Beutler T, Wiese D, Bassily N, Yee C. A multicenter trial of
sentinel lymph node mapping in colorectal cancer:
prognostic implications for nodal staging and recurrence. Am J Surg,
2006; 191:305-310.
7. Morton DL, Wen DR, Wong JH, Economou JS, Cagle
LA, Storm FK, Foshag LJ, Cochran AJ. Technical details
of intraoperative lymphatic mapping for early stage
melanoma. Arch Surg, 1992; 127:392-399.
8. Wainstein AJA, Barroso AA, Belfort AF. Significado
do linfonodo-sentinela no câncer do aparelho digestivo.
Tópicos em gastroenterologia 14. Editora Medsi, Rio de Janeiro,
RJ, 2004.
9. Hensen DE, Hutter RV. American Joint Commettee for
Cancer. In: Behars OH, Myers MH. Manual for staging of
cancer. Philadelphia: JB Lippincot, 1988, pp 75-80.
10. Sprung J, Tully MJ, Ziser A. Anaphilatic reactions to
isosulfan blue dye during sentinel node lymphadenectomy for
breast cancer. Anesth Analg, 2003; 96:1051-1053.
11. Nastro P, Sodo M, Dodaro CA, Gargiulo S, Acampa W,
Bracale U, Renda A. Intraoperative radiochromoguided mapping
of sentinel lymph node in colon câncer. Tumori, Milão,
v.88: p.352-353, 2002.
12. Saha S, Dan AG, Berman B, Wiese D, Schochet E, Barber
K, Choudhri S, Kaushal S, Ganatra B, Desai D, Nagaraju
M, Mannam S. Lymphazurin 1% versus 99mTc sulfur colloid
for lymphatic mapping in colorectal tumors: a
comparative analysis. Ann Surg Oncol, 2004; 11:21-26.
13. Paramo JC, Summerall J, Poppiti R, Mesko TW. Validation
of sentinel node mapping in patients with colon cancer. Ann
Surg Oncol, 2002; 9:550-554.
14. Basílio P, Fonseca LMB. Detecção de linfonodo-sentinela
no câncer colorretal. Arq Gastroenterol, 2006; 43:163-167.
15. Saha S, Dan AG, Beutler T, Wiese D, Badin J, Branigan
T, Peter Ng, Bassily N, David D. Sentinel lymph node
mapping technique in colon cancer. Semin Oncol, 2004; 31:374-381.
16. Patten LC, Berger DH, Bigas MR, Mansfield P,
Delpassand E, Cleary KR, Fagan SP, Curley SA, Hunt KK, Feig BW.
A prospective evaluation of radiocolloid and immunohistochemical staining in colon carcinoma
lymphatic mapping. Cancer, 2004; 100:2104-2109.
17. Doekhie FS, Peeters KCMJ, Kuppen PJK, Mesker WE,
Tanke HJ, Morreau H, Velde CHJ, Tollenaar RAEM. The
feasibility and reliability of sentinel node mapping in colorectal
cancer. Eur J Soc Oncol, 2005; 31:854-862.
18. De Haas RJ, Wicherts DA, Hobbelink MGG, Rinkes
IHMB, Schipper MEI, van der Zee J, Hillegersberg R. Sentinel
lymph node mapping in colon cancer: current status. Ann Surg
Oncol, 2007; 14:1070-1080.
19. Dess Guetz G, Uzzan B, Nicolas P, Cucherat M, Mestier
P, Morere JF, Breau JL, Perret G. Is sentinel lymph node
mapping in colorectal cancer a future prognostic factor? A
meta-analysis. World J Surg, 2007; 31:1304-1312.
20. Feig BW, Curley S, Lucci A, Hunt KK, Vauthey JN,
Mansfield PF, Cleary K, Hamilton S, Ellis V, Brame M, Berger DH.
A caution regarding lymphatic mapping in patients with
colon cancer. Am J Surg, 2001; 182:707-712.
21. Merrie AEH, van Rij A, Phillips L, Rossaak J, Yun K,
McCall JL. Diagnostic use of sentinel node in colon cancer. Dis
Colon Rectum, 2001; 44:410-417.
22. Viehl CT, Hamel CT, Marti WR, Guller U, Eisner
L, Stammberger U, Terracciano L, Spichtin HP, Harder F,
Zuber M. Identification of sentinel lymph nodes in colon
cancer depends on the amount of dye injected relative to tumor
size. World J Surg, 2003, 27:1285-1290.
23. Greene FL. American Joint Commettee on Cancer:
cancer staging handbook, TNM classification of malignant
tumors. New York: Springer-Verlag, 2002.
24. Benson AB, Schrag D, Somerfield MR, Cohen AM,
Figueredo AT, Flynn PJ, Krzyzanowska MK, Maroun J, McAllister
P, Cutsem EV, Brouwers , Charette M, Haller DG.
American society of clinical oncology recommendations on
adjuvant chemotherapy for stage II colon cancer. J Clin Oncol,
2004; 22:3408-3419.
25. Rossi BM, Bepu Jr P, Ferreira FO, Santos EMM, Aguiar Jr
S, Nakagawa WT, Lopes A. Number of dissected lymph
nodes in colorectal cancer patients submitted to radical surgery:
the quality of oncology treatment. Applied Cancer Research,
2006; 26:27-33.
26. Tuech JJ, Pessaux P, Regenet N, Bergamaschi R, Colson
A. Sentinel lymph node mapping in colon cancer. Surg
Endosc, 2004; 18:1721-1729.
27. Tiffet O, Kaczmarek D, Chambonierre MR, Guillan T,
Baccot S, Prevot N, Bageacu S, Bourgeois E, Cassagnau E, Lehur
PA, Dubois F. Combining radioisotopic and blue-dye
technique does not improve the false-negative rate in sentinel
lymph node mapping for colorectal cancer. Dis Col Rectum,
2007; 50:962-970.
28. Kitagawa Y, Watanabe M, Hasegawa H, Yamamoto S, Fujii
H, Yamamoto K, Matsuda J, Mukai M, Kubo A, Kitajima
M. Sentinel node mapping for colorectal cancer with
radioactive tracer. Dis Colon Rectum, 2002; 45:1476-1480.
29. Joosten JJA, Strobbe LJA, Wauters CAP, Pruszczynski
M, Wobbes T, Ruers TJM. Intraoperative lymphatic
mapping and the sentinel node concept in colorectal carcinoma. Br
J Surg, 1999; 86:482-486.
30. Paraf F, Sabourin JC. Optimal lymph node number and
occult lymph node metastases in colorectal cancer: the
pathologists view. Gastroenterol Clin Biol, 2000; 24:423-459.
31. Tschmelitsch J, Klimstra DS, Cohen AM. Lymph
node micrometastases do not predict relapse in stage II colon
cancer. Ann Surg Oncol, 2000; 7:601-608.
32. Cohen AM, Tremiterra S, Candeh F. Adjuvant therapy
for colorectal cancer. Curr Prob Cancer, 1998; 22:5-65.
33. Codignola C, Zorzi F, Mutti S, Rizzi A, Padelecchia E,
Morandi GB. Is there any role for sentinel node mapping in
colorectal cancer staging? Personal experience and review of the
literature. Jpn J Clin Oncol, 2005; 35:645-650.
34. O'Brien MJ. Immunocytochemical localization
of carcinoembryogenic antigen in benign and malignant
colorectal tissues. Assesment of diagnostic value. Am J Clin
Pathol, 1981; 75:283-290.
35. Huvus AG, Hutter RV, Berg JW. Significance of
axillary macrometastases and micrometastases in mammary
cancer. Ann Surg, 1971; 173:44-46.
36. Wong JH, Johnson DS, Namike P, Tauchi NP. Validation of
ex vivo lymphatic mapping in hematoxylin-eosin
node-negative carcinoma of the colon and rectum. Ann Surg Oncol,
2004; 11:772-777.
37. Bembenek AE, Schineider U, Gretschel S, Fisher J.
Detection of lymph node micrometastases and isolated tumor cells
in sentinel and nonsentinel lymph nodes of colon cancer
patients. World J Surg, 2005; 29:1172-1175.
38. Bendavid Y, Latulippe F, Younan RJ, Leclerc YE, Dube
S, Heyen F, Morin M, Girard R, Bastien E, Ferreira J,
Cerino M, Dube P. Phase I study on sentinel lymph node
mapping in colon cancer: a preliminary report. J Surg Oncol,
2002; 79:81-84.
Endereço para correspondência:
Antônio Hilário Alves Freitas
Rua Paracatu, 838 / 206 - Barro Preto
30180.090 - Belo Horizonte - Minas Gerais
Telefone e FAX: 31-3337.9988 Celular: 31-9956.1363
E-mail: hilariofreitas@ig.com.br
Recebido em 07/04/2008
Aceito para publicação em 22/04/2008
Trabalho realizado na Universidade Federal de Minas Gerais (UFMG); Fundação Hospitalar do Estado de Minas Gerais (FHEMIG); Fundação de Amparo à Pesquisa do Estado de Minas Gerais (FAPEMIG); Instituto de Pesquisa Biocâncer.