ARTIGOS ORIGINAIS
PROCESSO INFLAMATÓRIO EM MUCOSA DE RESERVATÓRIOS ILEAIS DE DOENTES ASSINTOMÁTICOS
Inflammatory Activity of Pelvic Ileal Pouches Mucosa in Asymptomatic Patients
Raquel Franco Leal1; Maria de Lourdes Setsuko Ayrizono2; Marciane Milanski3; João José Fagundes4; Andressa Coope3; Sandro Nunes Ângelo5; Lício Augusto Velloso6; Cláudio Saddy Rodrigues Coy4
1 Mestre em Cirurgia, Residência Médica em Coloproctologia pela Universidade Estadual de Campinas (UNICAMP); 2 Professor Doutor, Grupo de Coloproctologia - DMAD - UNICAMP; 3 Pós-graduação em Clínica Médica pela UNICAMP; 4 Professor Livre Docente, Grupo de oloproctologia, DMAD-UNICAMP; 5 Mestre em Cirurgia - Grupo de Coloproctologia, DMAD - UNICAMP; 6 Professor Associado, Departamento de Clínica Médica, FCM-UNICAMP.
RESUMO: A inflamação inespecífica do reservatório ileal (RI) após retocolectomia total é a complicação pós-operatória mais comum nos doentes operados por retocolite ulcerativa inespecífica (RCUI). Os mecanismos imunológicos envolvidos na etiologia não são totalmente conhecidos. Objetivo: Avaliar a ativação de STAT-1 e a expressão da citocina INF-g em mucosa de RI endoscópica e histologicamente normal, de doentes operados por RCUI e PAF, assintomáticos. Casuística e Método: Estudou-se 18 doentes submetidos à retocolectomia total com RI em "J", sendo nove com RCUI e nove com polipose adenomatosa familiar (PAF). Realizou-se biópsias da mucosa dos RI e de íleo terminal. As expressões de INF-g e a ativação de STAT-1 foram avaliadas por meio de imunoblot de extrato protéico total. Resultados: A ativação de STAT-1 foi maior em mucosa de RI de doentes operados por RCUI, quando comparada aos grupos PAF e Controle (p<0.05). A expressão de INF-g foi maior no grupo RCUI quando comparada ao grupo Controle (p<0.05), mas não em relação ao grupo PAF (p>0.05). Conclusão: Estes achados podem justificar a maior susceptibilidade dos doentes com RCUI à inflamação inespecífica do RI quando comparados aos portadores de PAF, sendo a principal via inflamatória similar à verificada na RCUI.
Descritores: Retocolite ulcerativa, polipose adenomatosa familiar, reservatório ileal, bolsa ileal, bolsite, citocinas.
INTRODUÇÃO
Retocolectomia total com confecção do
reservatório ileal (RI) é o procedimento de escolha para
doentes com retocolite ulcerativa inespecífica (RCUI)
com intratabilidade clínica, e para aqueles com
polipose adenomatosa familiar (PAF) que apresentam, em
geral, mais que vinte pólipos
retais.1,2,3,4,5,6 Entretanto, a inflamação inespecífica primária do RI ("bolsite") é uma
das complicações mais comuns após este procedimento
principalmente em RCUI, atingindo até 60% de
ocorrência, enquanto que apenas 5% dos portadores de PAF a
apresentam.7,8,9,10,11 A etiologia não é totalmente
esclarecida e o diagnóstico é clínico, porém deve ser
confirmado pelos achados endoscópicos e
histológicos.12-22
A diferença da incidência de "bolsite" entre
os doentes com RCUI e PAF tem levado alguns autores
à hipótese de que possa haver similaridade entre
esta complicação e a própria doença inflamatória
intestinal de base. 23,24
As citocinas pró-inflamatórias e as vias de
sinalização celular envolvendo o grupo de
proteínas ativadoras de transcrição nuclear (STAT)
apresentam papel importante na etiopatogenia da RCUI.
Especificamente, níveis elevados de
Interferon-ã (INF-g) e STAT-1 foram detectados em amostras de mucosa
intestinal de doentes portadores de doença
inflamatória intestinal, particularmente em
RCUI.25-30 No entanto, poucos estudos têm avaliado o processo
inflamatório em mucosa de RI com ileíte do reservatório e nas
condições de doentes
assintomáticos7,31-37, e
determinado se há correlação com a
RCUI.38-42
Assim, com a finalidade de avaliar o processo inflamatório em mucosa de RI de doentes
operados por RCUI e PAF com o trânsito íleoanal
reconstruído, assintomáticos, determinou-se a expressão da
citocina pró-inflamatória IFN-g e do fator de transcrição
nuclear do TNF-a, STAT-1, comparando-os nas
condições de doença acima citadas, e em grupo controle.
CASUÍSTICA E MÉTODOS
Biópsias de mucosa de RI foram obtidas de
nove doentes portadores de RCUI assintomáticos, com
média de idade de 48,7 (31-63) anos, sendo 55,6% do
sexo feminino, e de nove portadores de PAF,
também assintomáticos com média de idade de 33,8 (21-59)
anos e 55,6% do sexo feminino. O tempo de seguimento
pós-operatório foi de 73,1 (24-168) meses. Os
reservatórios ileais foram do tipo "J", e a arcada vascular do
cólon direito foi preservada como complementação à
irrigação sanguínea do íleo
terminal.43 A mucosectomia foi realizada e a anastomose íleo-anal foi
confeccionada manualmente. Os pacientes haviam sido submetidos
à reconstrução de trânsito, com fechamento da
ileostomia de proteção há mais de um ano. A ausência de ileíte
do RI foi observada clinicamente, além da
análise endoscópica e histológica realizada de acordo com
o Índice de Atividade da Ileíte do RI, proposto por
Sandborn e col 20. O grupo controle foi composto por nove
indivíduos com íleo-colonoscopia normal, sendo a média
de idade de 40,9 (26-58) anos e 55,6% do sexo
feminino. As biópsias foram obtidas do íleo distal.
O estudo foi realizado pelo Grupo de Coloproctologia e Laboratório de Sinalização
Celular da Universidade Estadual de Campinas e aprovado
pelo comitê de ética local registrado sob
no 543/2005 com adendo em 2007. Todos os pacientes assinaram o
termo de consentimento informado.
Fragmentos de íleo do RI e de íleo
terminal foram congelados em nitrogênio líquido, e
armazenados a -80oC, no Laboratório de Sinalização Celular
- FCM UNICAMP, para posterior homogeneização
em tampão de imunoprecipitado contendo 1% de
Triton X 100, 100mM de Tris (ph 7,4), 100mM de
pirofosfato de sódio, 100mM de fluoreto de sódio, 10mM
de EDTA, 10mM de vanadato de sódio, 2mM de
PMSF e 0,1mg/ml de aprotinina a 40C. O homogeneizado
foi então centrifugado à 11.000 rpm por 20 minutos.
No sobrenadante foi determinada a concentração de
proteína utilizando o método de Bradford
44, e posteriormente preparou-se amostra contendo 100ìg para
separação por SDS-PAGE. As amostras foram
diluídas em tampão de Laemmli, contendo 100mmol/L
de DTT. Após rápida fervura, foram aplicadas em
gel de poliacrilamida para separação por
eletroforese (SDS-PAGE). As proteínas separadas em
SDS-PAGE foram transferidas para membrana de nitrocelulose, em aparelho de transferência da
BIO-RAD. A membrana de nitrocelulose foi incubada "overnight" com 10ìl de anticorpo específico
(anti-IFN-g, anti-STAT-1). A ligação do anticorpo a
proteínas não-específicas foi minimizada pela
pré-incubação da membrana de nitrocelulose com
tampão de bloqueio (5% de leite em pó desnatado; 10
mmol/L de Tris; 150 mmol/L de NaCl; 0,02% de Tween 20) por 1,5
hora.45,46
Os reagentes para separação das proteínas
em gel de poliacrilamida e imunoblot foram da
Bio-Rad Laboratories (Richmond, CA). Aprotinina, Triton
X-100, Tween 20, glicerol foram adquiridos da Sigma (St.
Louis, MO). O papel de nitrocelulose (BA85,
0.2ìm) foi da Amersham (Aylesbury, UK). Os anticorpos
anti-phospho-STAT-1 (sc-7988, goat policlonal) e
anti-IFN-ã (sc-9344, goat policlonal) foram adquiridos da
Santa Cruz Biotechnology, Inc. (Santa Cruz, CA).
O sinal foi detectado por meio de reação
de quimioluminescência utilizando os reagentes
da SuperSignal®West Pico Chemiluminescent
Substrate da Pierce Biothecnology, Inc. Rockford. As
bandas autoradiografadas foram quantificadas por meio
de densitometria óptica (Gel-Pro Analyzer 3.1 software
- Exon-Intron Inc., Farrell, MD).
Os resultados foram notificados como
média com variação do erro padrão. Utilizou-se análise
de variância, seguida de teste de Tukey-Kramer para
comparações múltiplas de médias. Nível de
significância de p<0,05.
RESULTADOS
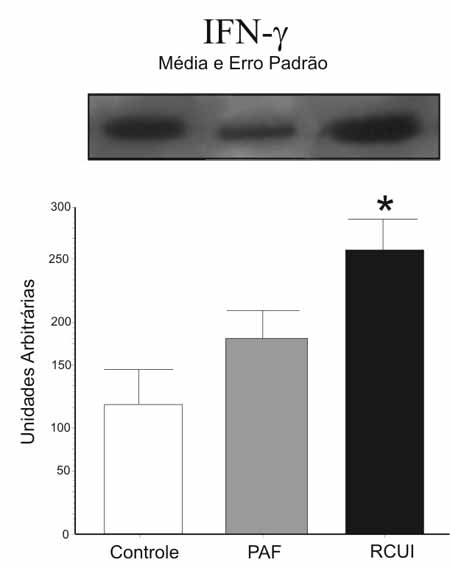
A análise das bandas auto-radiografadas
por meio de densitometria óptica mostrou os seguintes
dados arbitrários em relação à expressão de
IFN-g e à ativação de STAT-1 nos diferentes grupos (RCUI,
PAF e Grupo Controle), conforme as figuras ao lado.
 |
Figura 1 - Expressão de INF-g em mucosa de reservatório
ileal normal dos Grupos Controle, PAF e RCUI. Para todas as condições, n=09, *p<0.05 vs Control; § p<0.05 vs FAP. |
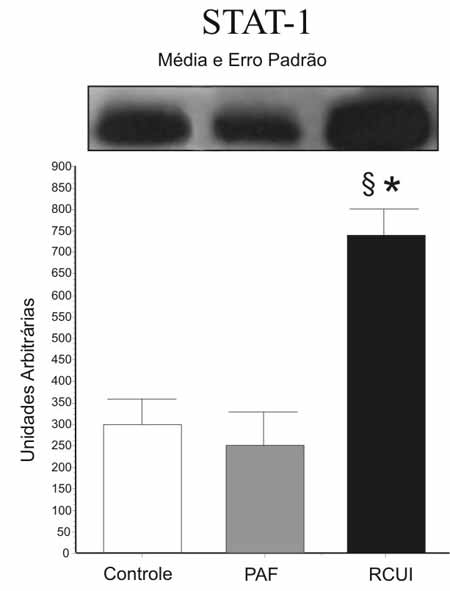 |
Figura 2 - Ativação de STAT-1 em mucosa de reservatório
ileal normal dos Grupos Controle, PAF e RCUI. Para todas as
condições, n=09, *p<0.05 vs Control; § p<0.05 vs FAP. |
ABSTRACT: Pouchitis after total retocolectomy is the most common complication in ulcerative colitis (UC). The immunological mechanisms involved in the genesis of pouchitis are unclear. Purpose: To evaluate STAT-1 activation and IFN-ã expression in normal ileal pouch mucosa. Methods: Eighteen asymptomatic patients submitted to total retocolectomy and J pouch, were evaluated, being nine with UC and nine with FAP. The activation of STAT-1 and expressions of the cytokine were determined by immunoblot of total protein extracts from pouch mucosal biopsies. Results: STAT-1 activation was increased in UC, when compared to FAP and controls. Higher levels of IFN-g expression were observed in UC when compared to control group, but was similar to FAP. Conclusions: These findings could explain a higher susceptibility to this inflammatory complication in UC when compared to FAP, which may be similar to UC disease.
Key Words: Ulcerative colitis, familial adenomatous polyposis, ileal pouch, pouchitis, cytokines.
Referências
1. Parks AG, Nicholls RJ. Proctocolectomy without
ileostomy for ulcerative colitis. Br Med J 1978;2:85-87
2. Utsunomiya J, Iwama T, Imajo M, et al. Total
colectomy, mucosal proctectomy, and ileoanal anastomosis. Dis
Colon Rectum 1980;23:459-466
3. Nicholls RJ, Moskovitz RL, Shepard NA.
Restorative proctocolectomy with ileal
reservoir. Br J Surg 1985;72:76-79
4. Nicholls RJ. Restorative proctocolectomy with various
types of reservoir. World J Surg 1987;11:751-762
5. M'Koma AE. Serum biochemical evaluation of patients
with functional pouches tem to 20 years after
restorative proctocolectomy. Int J Colorectal Dis 2006;26:1-10
6. Mc Guire BB, Brannigan AE, O'Connell PR. Ileal
pouch-anal anastomosis. Br J Surg 2007;94:812-23
7. Kiehne K, Brunke G, Wegner F, et al. Defensin expression
in chronic pouchitis in patients with ulcerative colitis or
familial adenomatous polyposis coli. World J
Gastroenterol 2006;21:12(7):1056-1062
8. Heuschen UA, Allemeyer EH, Hinz U, et al.
Diagnosing pouchitis: comparative validation of two scoring system
in routine follow-up. Dis Colon Rectum 2002;45(6):776-786
9. Shen B, Fazio VW, Renzi FH, et al. Risk factors for disease
of ileal pouch-anal anastomosis after restorative
proctocolectomy for ulcerative colitis. Clin Gastroenterol Hepatol
2006;4(1):81-89
10. Moskowitz RL, Shepard NA, Nicholls RJ. An assessment
of inflammation in the reservoir after restorative
proctocolectomy with ileoanal ileal reservoir. Int J Colorectal Dis
1986;1:167-174
11. Meagher AP, Farouk R, Dozois RR, et al. J ileal
pouch-anal anastomosis for chronic ulcerative colitis: complications
and long-term outcome in 1310 patients. Br J Surg
1998;85:800-803
12. Armstrong DN, Sillin LF, Chung R. Reduction in tissue
blood flow in J-shaped pelvic ileal reservoirs. Dis Colon
Rectum 1995;38:526-529
13. Laake KO, Bjorneklett A, Aamodt G, et al. Outcome of
four weeks's intervention with probiotics on symptoms
and endoscopic appearance after surgical reconstruction with a
J-configurated ileal-pouch-anal-anastomosis in ulcerative
colitis. Scand J Gastroenterol 2005;40:43-51
14. Ohge H, Furne JK, Springfield J, et al. Association
between fecal hydrogen sulfide production and pouchitis. Dis
Colon Rectum 2005;48:469-475
15. Kuehbacher T, Ott SJ, Helwig U, et al. Bacterial and
fungal microbiota in relation to probiotic therapy in pouchitis.
Gut 2006;55(6):833-841
16. Sandborn WJ. Pouchitis following ileal pouch anal
anastomosis: definition, pathogenesis, and treatment.
Gastroenterology 1994;107:1856-1860
17. Nicholls RJ, Banerjee AK. Pouchitis: risk factores,
etiology, and treatment. World J Surg 1998;22:347-356
18. Kienle P, Weitz J, Reinshagen S, et al. Association of
decreased perfusion of the ileoanal pouch mucosa with
early postoperative pouchitis and local septic complications.
Arch Surg 2001;136:1124-30
19. Heuschen G, Leowardi C, Hinz U, et al. Differential
expression of toll-like receptor 3 and 5 in ileal pouch mucosa of
ulcerative colitis patients. Int J Colorectal Dis 2007;22:293-301
20. Sandborn WJ, Tremaine WJ, Batts KP, et al. Pouchitis
after ileal pouch-anal anastomosis: a Pouchitis disease
activity Index. Mayo Clin Proc 1994;69:409-415
21. Shen B, Achkar JP, Connor JT, et al. Modified
Pouchitis Disease Activity Index. A simplified approach to the
diagnosis of pouchitis. Dis Colon Rectum 2003;46(6):748-753
22. Akerlung JE, Lofberg R. Pouchitis. Curr Opin
Gastroenterol 2004;20(4):341-344
23. Lohmuller JL, Pemberton JH, Dozois RR, et al. Pouchitis
and extraintestinal manifestations of inflammatory bowel
disease after ileal pouch-anal anastomosis. Ann Surg
1990;211(5):622-629
24. Hata K, Watanabe T, Shinozaki M, et al. Patients
with extraintestinal manifestations have a higher risk of
developing pouchitis in ulcerative colitis: multivariate analysis. Scand
J Gastroenterol 2003;38:1055-1058
25. O'Shea J, Ma A, Lipsky P. Cytokines and
autoimmunity. Nature Reviews 2002;2:37-45
26. Mudter J, Weigmann B, Bartsch B, et al. Activation pattern
of signal transducers and activators of transcription
(STAT) factors in inflammatory bowel disease. Am J
Gastroenterol 2005;100:64-72
27. Pullman WE, Elsbury S, Kobayashi M, et al. Enhanced
mucosal cytokine production in inflammatory bowel disease.
Gastroenterology 1992;102:529-537
28. Schreiber S, Rosenstiel P, Hampe J, et al. Activation of
signal tranducer and activator of transcription (STAT) 1 in
human chronic inflammatory bowel disease. Gut 2002;51:379-385
29. Klampfer L, Huang J, Sasazuki T, et al. Inhibition of
Interferon g signaling by the short chain fatty acid butyrate. Mol
Cancer Res 2003;1:855-62
30. Schreiber S, Hampe J, Nikolaus S, et al. Patterns of
cytokine transcription factor activation are different in Crohn's
disease (CD) and ulcerative colitis (UC).
Gastroenterology 1997;112(4):A1086
31. Gionchetti P, Campieri M, Belluzzi A, et al.
Mucosal concentrations of interleukin-1 beta, interleukin-6,
interleukin-8, and tumor necrosis factor-alpha in pelvic ileal pouches.
Dig Dis Sci 1994;39:1525-1531
32. Evgenikos N, Bartolo DCC, Hamer-Hodges DW, et
al. Assessment of ileoanal pouch inflammation by
interleukin 1â and interleukin 8 concentrations in the gut lumen. Dis
Colon Rectum 2002;45:249-255
33. Bulois P, Tremaine WJ, Maunoury V, et al. Pouchitis
is associated with mucosal imbalance between interleukin-8
and interleukin-10. Inflamm Bowel Dis 2000;6:157-167
34. Lammers KM, Vergopoulos A, Babel N, et
al Probiotic therapy in the prevention of pouchitis onset: decreased
Interleukin-1â, Interleukin-8 and Interferon-ã gene expression.
Inflamm Bowel Dis 2005;11(5):447-454
35. Schmidt C, Giese T, Ludwig B, et al. Increased
cytokine transcripts in pouchitis reflect the degree of inflammation
but not the underlying entity. Int J Colorectal Dis
2006;21:419-426
36. Helwig U, Gionchetti P, Rizello F, et al. CXC and
CC chemokine expression in inflamed and noninflamed pelvic
ileal pouch tissue. Int J Colorectal Dis 2004;19:165-170
37. Ulisse S, Gionchetti P, D'Aló S, et al. Expression of
cytokines, inducible nitric oxide synthase, and matrix
metalloproteinases in pouchitis: Effects of probiotic treatment. Am J
Gastroenterol 2001;96(9):2691-9
38. Kuhbacher T, Gionchetti P, Hampe J, et al. Activation
of signal-transducer and activator of transcription 1(STAT1)
in pouchitis. Clin Exp Immunol 2001;123:395-401
39. Boerr L, Sambuelli A, Sugay E, et al. Serum
TGF-â1 and Interferon _ã levels in ileal pouch-anal anastomosis in
ulcerative colitis. Gastroenterology 1998;114:A936
40. Schreiber S, Gionchetti P, Hampe J, et al. Pouchitis
shares similarities with ulcerative colitis in the pattern of
cytokine transcription factor activation.
Gastroenterology 1997;112(4):A1086
41. Stallmach A, Schafer F, Hoffmann S, et al.
Increased state of activation of CD4 positive T cells and elevated interferon
ã production in pouchitis. Gut 1998;43:499-505
42. Patel RT, Bain I, Youngs D, et al. Cytokine production
in pouchitis is similar to that in ulcerative colitis. Dis
Colon Rectum 1995;38:831-837
43. Góes JRN, Coy CSR, Amaral CA, et al. Superior
mesenteric artery symdrome as a complication of ileal
pouch-anal anastomosis. Dis Colon Rectum 1995;38:543-4
44. Bradford MM. A rapid and sensitive method for
the quantitation of microgram quantities of protein utilizing
the principle of protein-dye binding. Anal Biochem
1976;72:248-254
45. Velloso LA, Folli F, Sun XJ, et al. Cross-talk between
the insulin and angiotensin signaling systems. Proc Natl Acad
Sci USA 1996;93:12490-12495
46. Araújo EP, De Souza CT, Gasparetti AL, et al. Short-term
in vivo inhibition of insulin receptor substrate-1 expression
leads to insulin resistence, hyperinsulinemia, and increased
adiposity. Endocrinology 2005;146:1428-1437
47. Kuhbacher T, Schreiber S, Runkel N.
Pouchitis: pathophysiology and treatment. Int J Colorectal
Dis 1998;13:196-207
48. Tulchinsky H, Hawley PR, Nicholls J. Long-term failure
after restorative proctocolectomy for ulcerative colitis. Ann
Surg 2003;238(2):229-234
49. Kuhn K, Lohler J, Rennick D, et al.
Interleukin-10-deficient mice develop chronic enterocolitis. Cell 1993;75:263-74
50. Chen LF, Greene WC. Shaping the nuclear action of
NF-B. Nature Reviews 2004;5:392-401
51. Schreiber S, Nikolaus S, Hampe J. Activation of nuclear
factor KB in inflammatory bowel disease. Gut 1998;42:477-84.
Endereço para correspondência:
Raquel Franco Leal
Rua Patativa, no 170, apto 24C
Bonfim - CEP 13034-810
Campinas, São Paulo
Tel. -19-32844803
raquelleal@mpc.com.br
ccoy@terra.com.br
Recebido em 17/09/2008
Aceito para publicação em 29/10/2008
Trabalho realizado pelo Grupo de Coloproctologia, Disciplina de Moléstias do Aparelho Digestório, (DMAD), Faculdade de Ciências
Médicas, Universidade Estadual de Campinas (UNICAMP), Campinas, São Paulo, Brasil. Laboratório de Sinalização Celular, Departamento de
Medicina Interna, Faculdade de Ciências Médicas, Universidade Estadual de Campinas (UNICAMP), Campinas, São Paulo, Brasil.