ARTIGOS ORIGINAIS
A PESQUISA DE SANGUE OCULTO NAS FEZES ASSOCIADA A UM QUESTIONÁRIO DE SINAIS E SINTOMAS NA PREVENÇÃO DO CÂNCER COLO RETAL
Faecal Occult Blood (FOB) Test Associated with a Questionaire of Signs and Symptoms in Screening for Colorectal Cancer
Francisco Luis Altenburg1, Maria de Lourdes Pessole Biondo-SimÕes2, Luis Carlos Von Bahten3
1 Mestrando do Programa de Pós-Graduação em Clínica Cirúrgica da PUCPR, Coordenador do Serviço de Coloproctologia do Hospital Regional Hans Dieter Schmidt, Joinville, Santa Catarina; 2 Professora Titular de Metodologia da Pesquisa da PUCPR e Professora Adjunto IV do Departamento de Cirurgia da Universidade Federal do Paraná. Membro da Sociedade Brasileira de Colo-Proctologia e Titular do Colégio Brasileiro de Cirurgiões (CBC); 3 Professor Coordenador e Orientador do Programa de Pós-Graduação em Clínica Cirúrgica da PUCPR, Membro Titular do CBC.
Resumo: OBJETIVO: Determinar a eficácia de um programa de prevenção de Câncer Colo Retal (CCR) através do método da pesquisa de sangue oculto das fezes (PSO), e um questionário clínico (QSA). Material e Método: Foi realizada uma triagem através do PSO e do QSA em indivíduos acima de 50 anos, oriundos de uma campanha de prevenção de CCR em Joinville, SC. 387 indivíduos aderiram à campanha e 93 foram excluídos.. Foram definidos 3 grupos: 1- PSO +, com 20 sujeitos, QSA +, com 38 sujeitos e PSO e QSA negativos com 21 sujeitos. Foi definida como colonoscopia positiva aquela que detectou adenomas. Resultados: O grupo 1 apresentou 22% de sensibilidade, 74% de especificidade, likelihood ratio positivo (LR) de 0, 9, acurácia de 56, 9, valor preditivo positivo (VPP) de 31,6 e negativo (VPN) de 64. O grupo 2 apresentou 71,4% de sensibilidade, 45,6 de especificidade, LR de 1,3, acurácia de 52,6, VPP de 32,6 e VPN de 81,3. O método apresentou 95,2% de sensibilidade, 63,2 de especificidade, LR de 2, 6, acurácia de 71, 8, VPP de 48.8 e VPN de 97.3. Conclusão: O método da PSO e QSA são complementares e efetivos como triagem em programas de prevenção de CCR.
Descritores: Neoplasias do Colon, Diagnóstico Colonoscopia, Anamnese, Promoçăo da Saúde.
INTRODUÇÃO
O câncer colo-retal (CCR) representa uma
das mais significantes e prevalentes causas de morte
por câncer no dias atuais. Nos Estados Unidos e no
Reino Unido é o terceiro tipo de câncer mais diagnosticado
e a segunda causa de morte por
câncer1.
No Brasil, para o ano de 2008, o Instituto
Nacional do Câncer (INCA) projetou 12.490 novos
casos em homens e 14.500 novos casos em mulheres,
ocupando a quarta e a terceira colocação
respectivamente2.
Programas de prevenção têm-se mostrado
efetivos na diminuição de mortalidade e incidência
por câncer colo-retal, sendo recomendados por várias
instituições proeminentes por todo o
mundo3. Apesar disto, os índices de participação permanecem baixos,
influenciando o custo efetividade dos
programas1, 3.
A colonoscopia é o melhor exame
preventivo, pois além de diagnosticar o CCR permite identificar
e tratar pólipos, lesões precursoras da doença, sendo
responsável pelo declínio da incidência do CCR, pós
1986, nos EUA4.
São necessários, porém métodos de
triagem para a realização de colonoscopias, pois mesmo
em países desenvolvidos não seria possível à realização
de colonoscopias em todos os indivíduos acima de 50
anos, porém o custo benefício da diminuição de
mortalidade pela detecção precoce das lesões precursoras
(pólipos), ou os crescentes achados de CCR em fase inicial
têm estimulado a realização destas
triagens3.
A maioria dos programas de prevenção de
CCR é baseada em triagens realizadas pela pesquisa de
sangue oculto nas fezes. Recente revisão sistemática
da Cochrane demonstrou que o rastreamento feito com
a pesquisa de sangue oculto nas fezes reduziu o
risco relativo para o CCR em 16%. A redução do risco
relativo de morte por CCR foi de 15%. Já a redução
do RR de morte em indivíduos de risco chegou a
25%1.
Recente metanálise reportou que a PSO
não teve impacto na mortalidade, nem foi
estatisticamente significante em relação às mortes por outras causas
na população triada. A maioria dos estudos revelou
alta porcentagem de falsos positivos. Para eles o
impacto da PSO na mortalidade é incerto e sua eficácia
no rastreamento do CCR necessita de
reavaliação5.
Outra metanálise de revisão de mortalidade
em grupos controlados de rastreamento de CCR,
realizado com PSO mostrou redução de mortalidade de
14% em 10 anos. Entretanto, o acompanhamento a
longo prazo não demonstrou
proteção6.
Quando se analisa o custo efetividade de
vários programas de prevenção verifica-se que a
maioria deles inclui indivíduos com mais de cinqüenta anos,
que apresentam risco aumentado para o CCR. A sigmoidoscopia flexível e a colonoscopia parecem
ter o melhor custo efetividade. Este fato é devido ao
conceito assumido de que praticamente todos os
CCR, provêm de adenomas, que podem ser
detectáveis7.
O segmento de indivíduos com potencial
risco para CCR, durante 11 anos, rastreados pelo PSO,
permitiu verificar que os programas de prevenção
baseados neste exame permitiram diminuir a incidência
da doença. Nos indivíduos que se recusaram a realizar
o exame a incidência de CCR foi maior. É bem
provável que entre os rastreados a incidência tenha sido
maior pela realização de maior número de colonoscopias
complementares. Neste estudo os autores utilizaram
um questionário de rastreamento8.
No Reino Unido, questionários baseados
em sintomas (WNS) têm sido utilizados para abreviar
o tempo de espera para consultas com especialistas
em cirurgia colo-retal (fast track referral)l. Vários
estudos foram feitos e verificaram a efetividade deste
sistema de referência e recomendaram a continuação
do programa. Estudos que relatam a importância de
se coletar dados em um programa de rastreamento de CCR como: sintomas, história familiar, pessoal e
fatores de risco, comprovam que esta coleta de dados
aumenta a adesão a programas de prevenção com a
pesquisa de sangue oculto nas fezes9,
10.
A ideia de coletar informações de sintomas
e antecedentes não é nova. Keddie e Hargreaves,
em 1968, já reconheceram que não havia relação entre
o início de sintomas e o estádio do CCR, e que a
presença de sintomas sistêmicos eram
comuns11. Outros estudos avaliam o tempo de evolução dos
sintomas até a descoberta do
CCR12, a presença de sintomas precoces nos indivíduos com adenomas e CCR, e
a importância da história familiar nos programas de
prevenção 13,14.
A hipótese de que a descoberta de
lesões neoplásicas do cólon e reto poderia ser
incrementada com um questionário abordando sinais, sintomas e
antecedentes, entre nós, foi levantada a partir de um
estudo piloto no qual se analisou os resultados de colonoscopias em indivíduos com PSO positivo e
negativo. Aquele estudo revelou que a maioria dos
indivíduos triados e com colonoscopia positiva já eram
sintomáticos15.
OBJETIVO
O objetivo deste trabalho foi verificar a
eficácia e acurácia da PSO associada a um
questionário clínico (QSA), com enfoque em sintomas de alarme
do CCR, como meio de triagem para o diagnóstico
de neoplasias do cólon e reto.
MÉTODOS
O projeto que deu origem a este estudo obedeceu a Resolução do Conselho Nacional de Saúde
196/96 e foi avaliado e aprovado pela Comissão de
Ética do Hospital Regional de Joinville, com o número 08009.
A população estudada foi proveniente de
uma triagem realizada em uma campanha de prevenção
do câncer do cólon e reto, em que foram atingidos
por correspondência direta, fôlderes e por meios de
comunicação, aproximadamente 10.000 pessoas acima
dos 50 anos de idade, de ambos os sexos, usuárias de
um plano de saúde local, que voluntariamente aderiram
ao programa de prevenção.
A pesquisa clínica foi realizada nas
instalações de um centro hospitalar (CHU), de um plano de
saúde local. No período de 21 de novembro a 10 de
dezembro de 2007 foi realizada a campanha de prevenção
do CCR durante a qual foram preenchidos os
questionários (QSA) e realizados os exames de PSO. Foram
excluídos do estudo os sujeitos que já tinham
realizado colonoscopia anteriormente.
O método da PSO utilizado foi o imunocromatográfico para todas as amostras
examinadas.
O detalhamento do QSA está no anexo
1. Este foi considerado positivo para dois critérios:
1- quando da existência de antecedentes
familiares, isto é, a presença de pelo menos um
familiar, de primeiro grau, com CCR ou adenomas;\
2- quando da existência de sintomas
2a- específicos - Sangue misturado às fezes
e/ou alteração de hábito intestinal por mais de três
meses para mais frequente, fezes finas e, ou perda
de fezes (estes dois sintomas isolados determinavam
um QSA positivo),
2b- não específicos - dor abdominal
em hipogástrio por mais de três meses, anemia sem
causa definida, astenia, dor retal e sensação de
evacuação incompleta.
Nos casos de sintomas não específicos o
QSA foi considerado positivo quando havia a associação
de pelo menos dois sintomas.
A partir da análise do QSA e dos resultados
da PSO foram definidos três grupos:
Grupo 1- Indivíduos com PSO positiva;
Grupo 2- Indivíduos com QSA positivo;
Grupos 3- Voluntários com PSO negativa e QSA negativo.
Foram realizadas colonoscopias nos pacientes dos três grupos que foram feitas nas instalações
do CHU, sob sedação profunda, com
acompanhamento de um anestesiologista. Para a sedação foi
utilizado Propofol (1 µg/Kg), fentanil (1 µg/Kg) e Midazolan
(1 a 2 MG/kg). Os endoscópios utilizados foram da
marca Olympus®
Foi definida como colonoscopia positiva aquelas que detectaram lesões neoplásicas do cólon e/
ou reto. Este exame foi utilizado como controle do PSO
e do QSA.
Os dados foram colocados no programa de banco de dados Excel e analisados pelo programa
de análise estatística 1.8 para Windows®,
reconhecendo-se a sensibilidade, a especificidade, os valores
preditivos positivo e negativo, o likelihood ratio
e a acurácia dos exames nos grupos de estudo.
RESULTADOS
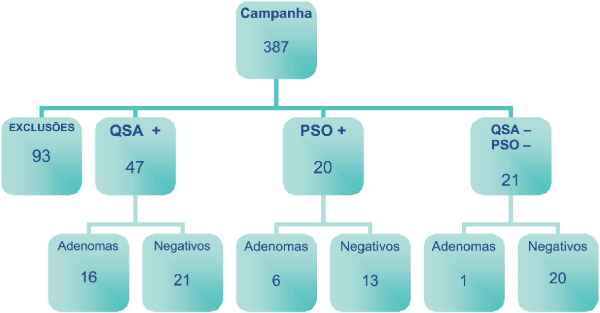
Aderiram ao estudo 387 indivíduos. Destes
93 foram retirados do estudo por apresentarem
critérios de exclusão. Restaram para análise 294 indivíduos,
138 (46,93%) do sexo masculino e 156 do sexo
feminino (53,03%). A média de idade foi 59,02 ± 14,42 anos.
A idade mínima foi de 50 anos e a máxima foi de 90
anos. A idade, o peso e o índice de massa corpórea
(IMC) em cada um dos grupos foram semelhantes, o que
deu caráter homogêneo à amostra estudada.
Para uma população estimada de 10.000
nesta faixa etária, o grau de adesão ao programa foi de
apenas 3,87%.
Após a análise do questionário
estabeleceram-se os participantes de cada grupo. No grupo 1
ficaram 20 indivíduos, no grupo 2 restaram 47 e no grupo 3,
21 participantes.
Foram realizadas 78 colonoscopias e todas alcançaram o íleo terminal. A distribuição dos
sujeitos da pesquisa, e os resultados das
colonoscopias estão descritos no organograma da figura 1.
 |
Figura 1 - Organograma demonstrativo da amostra e dos grupos de estudo. |
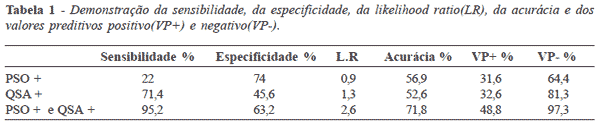 |
ABSTRACT: The purpose of this study is to verify the efficacy of a strategy to screen colorectal cancer(CCR) and adenomas using the faecal occult blood test(PSO) and a questionnaire (QSA)based in signs and symptoms of CCR. Methods: A program of prevention was done, and the patients answered the QSA and did the PSO type imunocromatograph. Results: 387 people adhered do the program, 93 were excluded. Three groups were formed: 1: 20 persons, with PSO positive, 2:38 persons with QSA positive, and 3, with 21 persons with PSO and QSA negatives. Group 1 presented a sensibility of 22%, specificity of 74%, Likelihood ratio + of 0,9, accuracy of 56,9, Positive predictive value(VPP) of 31,6 and negative(VPN) of 64. Group 2 presented sensibility of 71,4%, 45,6% of specificity, Likelihood ratio + 1.3, accuracy of 52,6, VPP de 32,6 e VPN de 81,3. The QSA plus PSO method, presented a sensibility of 95,2%, 63,2 of specificity, accuracy of 71,8 ,Likelihood ratio of 2,6, VPP de 48,8 e VPN 81,3. In conclusion the method of PSO and QSA are complementary and seem effective in screening for CCR in preventive programs.
Referências
1. Hewitson P, Glasziou P, Watson E, Towler B, Irwig
L. Cochrane systematic review of colorectal cancer screening
using the fecal occult blood test (hemoccult): an update. Am
J Gastroenterol. 2008; 103(6):1541-9.
2. Instituto Nacional do Câncer (INCA). Estimativas 2008
_ Incidência de câncer no Braisil. Disponível em:
http://www.inca.gov.br/estimativas/2008/mapa.asp?ID=6.
Acesso em: 7 Apr 2008.
3. Rothenberger DA, Dalberg DL, Leininger A.
Minnesota Colorectal Cancer Initiative: successful development
and implementation of a community-based colorectal
cancer registry. Dis Colon Rectum. 2004; 47(10):1571-7.
4. Nelson RL, Persky V, Turyk M. Determination of
factors responsible for the declining incidence of colorectal
cancer. Dis Colon Rectum. 1999; 42(6):741-52.
5. Moayyedi P, Achkar E. Does fecal occult blood testing
really reduce mortality? A reanalysis of systematic review data.
Am J Gastroenterol. 2006; 101(2):380-4.
6. Heresbach D, Manfredi S, D'halluin PN, Bretagne JF,
Branger B. Review in depth and meta-analysis of controlled trials
on colorectal cancer screening by faecal occult blood test. Eur
J Gastroenterol Hepatol. 2006; 18(4):427-33.
7. Pignone M, Rich M, Teutsch SM, Berg AO, Lohr KN.
Screening for colorectal cancer in adults at average risk: a summary
of the evidence for the U.S. Preventive Services Task Force.
Ann Intern Med. 2002; 137(2):132-41.
8. Niv Y, Lev-El M, Fraser G, Abuksis G, Tamir A.
Protective effect of faecal occult blood test screening for colorectal
cancer: worse prognosis for screening refusers. Gut. 2002; 50(1):33-7.
9. Selvachandran SN, Hodder RJ, Ballal MS, Jones P, Cade
D. Prediction of colorectal cancer by a patient
consultation questionnaire and scoring system: a prospective study.
Lancet. 2002; 360(9329):278-83.
10. Smith D, Ballal M, Hodder R, Soin G, Selvachandran
SN, Cade D. Symptomatic presentation of early colorectal
cancer. Ann R Coll Surg Engl. 2006; 88(2):185-90.
11. Keddie N, Hargreaves A. Symptoms of carcinoma of the
colon and rectum. Lancet. 1968; 2(7571):749-50.
12. Stubbs RS, Long MG. Symptom duration and pathologic
staging of colorectal cancer. Eur J Surg Oncol. 1986; 12(2):127-30.
13. Johns LE, Houlston RS. A systematic review and
meta-analysis of familial colorectal cancer risk. Am J Gastroenterol.
2001; 96(10):2992-3003.
14. Church JM. A scoring system for the strength of a
family history of colorectal cancer. Dis Colon Rectum.
2005; 48(5):889-96.
15. Altenburg FL, Biondo-Simões MLP, Santiago A. Pesquisa
de sangue oculto nas fezes e correlação com alterações
nas colonoscopias. Rev bras colo-proctol. 2007; 27(3): 304-9.
16. Levin B, Lieberman DA, McFarland B, Andrews KS,
Brooks D, Bond J, et al. American Cancer Society Colorectal
Cancer Advisory Group; US Multi-Society Task Force; American
College of Radiology Colon Cancer Committee. Screening and
surveillance for the early detection of colorectal cancer and adenomatous
polyps, 2008: a joint guideline from the American Cancer Society, the
US Multi-Society Task Force on Colorectal Cancer, and the
American College of Radiology. Gastroenterology. 2008; 134(5):1570-95.
17. Fang CB. Rastreamento do câncer colorretal. Rev Assoc
Med Bras. 2002; 48(4):286-6.
18. www.inca.gov.br. Câncer colo-retal. Acesso em 24 ago 2008.
19. American Cancer Society. Cancer facts and figures,
1999. Atlanta: American Cancer Society, 1999.
20. Screening for colorectal cancer using the faecal occult
blood test, Hemoccult. Cochrane Database Syst Rev. 2007
Jan 24;(1):CD001216.
21. Woo HY, Mok RS, Park YN, Park DI, Sung IK, Sohn CI,
Park H. A prospective study of a new immunochemical fecal
occult test in Korean patients referred for colonoscopy.
Clin Biochem. 2005; 38(4):395-9.
22. Anderson WF; Guyton KZ; Hiatt RA; Vernon SW; Levin
B; Hawk E. Colorectal cancer screening for persons at
average risk. J Natl Cancer Inst. 2002;94(15):1126-33.
23. Ward N.,Wright J,Marsh S,Norton J. Fast track referrals
for colorectal cancer: the impact of the faecal occult blood
test screening program.Colorectal Disease.2007;9(3):258-61.
24. Mandel JS, Bond JH, Church TR, Snover DC, Bradley
GM, Schuman LM, Ederer F. Reducing mortality from
colorectal cancer by screening for fecal occult blood. Minnesota
Colon Cancer Control Study. N Engl J Med. 1993; 328(19):1365-71.
25. Goodyear SJ, Stallard N, Gaunt A, Parker R, Williams
N, Wong L. Local impact of the English arm of the UK
Bowel Cancer Screening Pilot study. Br J Surg. 2008; 95(9):1172-9.
26. Trevena LJ, Irwig L, Barratt A. Randomized trial of a
self-administered decision aid for colorectal cancer screening.
J Med Screen. 2008; 15(2):76-82.
27. Sung JJ, Lau JY, Young GP, Sano Y, Chiu HM, Byeon JS et
al. Asia Pacific consensus recommendations for colorectal
cancer screening. Gut. 2008; 57(8):1166-76.
28. van Rossum LG, van Rijn AF, Laheij RJ, van Oijen MG,
Fockens P, van Krieken HH, et al. Random comparison of guaiac
and immunochemical fecal occult blood tests for colorectal cancer
in a screening population. Gastroenterology. 2008; 135(1):82-90.
29. Zavoral M. Colorectal cancer screening in the Czech
Republic. Z Gastroenterol. 2008; 46 Suppl 1:S29-30.
30. Zorzi M, Barca A, Falcini F, Grazzini G, Pizzuti R, Ravaioli
A et al. Screening for colorectal cancer in Italy: 2005
survey. Epidemiol Prev. 2007; 31(2-3 Suppl 2):49-60.
Endereço para correspondência:
Francisco Luis Altenburg
Rua 15 de novembro 2119, casa 14, Joinville, Santa Catarina
CEP 89201-620
Tel.: (047) 3422-9363 / (047) 9964-5837
E mai: progastro@terra.com.br
Recebido em 12/10/2008
Aceito para publicação em 29/10/2008
Trabalho desenvolvido como parte de dissertação de mestrado - Programa de Pós-Graduação em Clínica Cirúrgica da Pontifícia
Universidade Católica do Paraná (PUCPR).
 |